Bateria recarregable

Una pila o bateria recarregable (també anomenada acumulador) és un grup d'una o més cel·les electroquímiques secundàries. Les piles i bateries recarregables usen reaccions electroquímiques que són elèctricament reversibles, és a dir:
- Quan la reacció transcorre en un sentit, s'esgoten els materials de la pila mentre es genera un corrent elèctric.
- Quan la reacció transcorre en sentit invers, és necessari un corrent elèctric per regenerar els elements consumits.
Les bateries recarregables venen en diferents mides i fan servir diferents combinacions de productes químics. Les cel·les secundàries («bateria recarregable») utilitzades amb més freqüència són les de plom-àcid, la de níquel-cadmi (NiCd), la de níquel-metall hidrur (NiMH), la de ions de liti (Li-ió), i la de polímer d'ions de liti (polímer de Li -ió).
Les bateries recarregables poden oferir beneficis econòmics i ambientals en comparació amb les piles no recarregables. Alguns tipus de bateries recarregables estan disponibles en les mateixes mides que els models d'un sol ús. Encara que les piles recarregables tenen un major cost inicial, poden ser recarregades moltes vegades. La selecció adequada d'una bateria recarregable pot reduir els materials tòxics rebutjats en els abocadors, davant d'una sèrie equivalent de piles d'un sol ús. Per exemple, els fabricants de bateries o piles recarregables de NiMH proclamen una vida de servei de 100-1000 cicles de càrrega/descàrrega per a les seves bateries.
Usos i aplicacions
[modifica]

Les bateries recarregables actualment s'utilitzen per a aplicacions com ara motors d'arrencada d'automòbils, dispositius portàtils de consum, vehicles lleugers (com cadires de rodes motoritzades, carros de golf, bicicletes elèctriques i carretons elevadors elèctrics), eines i sistemes d'alimentació ininterrompuda. Noves aplicacions com la seva ocupació per a vehicles elèctrics híbrids i vehicles elèctrics estan impulsant la tecnologia per reduir costos, reduir el pes i augmentar de la vida útil.[1]
A diferència de les piles no recarregables (cel·les primàries), les bateries recarregables han de ser carregades abans del seu primer ús. La necessitat de carregar les piles recarregables abans del seu ús dissuadeix els possibles compradors que vulguin utilitzar les piles immediatament. No obstant això, les noves bateries de baixa auto descàrrega permeten als usuaris comprar una bateria recarregable que ja té prop del 70% de la seva capacitat nominal, permetent als consumidors utilitzar les bateries immediatament i regenerar (recarregar) més tard fins al 100% de la seva capacitat.
Aplicacions d'emmagatzematge d'energia en xarxa fan servir bateries recarregables industrials per a anivellament de càrrega, emmagatzemant l'energia elèctrica durant períodes de càrrega màxima per al seu posterior ús, i per aprofitament d'energies renovables, com ara l'emmagatzematge d'energia generada a partir de panells fotovoltaics durant el dia per a ser utilitzada durant la nit. En carregar les bateries durant els períodes de baixa demanda i tornar l'energia a la xarxa durant els períodes d'alta demanda elèctrica, l'anivellament de càrrega ajuda a eliminar la necessitat de costoses plantes d'energia en hores punta i ajuda a amortitzar el cost dels generadors durant les hores de més funcionament.
L'Associació Nacional de Fabricants Elèctrics dels Estats Units ha estimat que la demanda dels EUA per a piles recarregables està creixent dues vegades més ràpid que la demanda de les no-recarregables (d'un sol ús).[2]
Càrrega i descàrrega
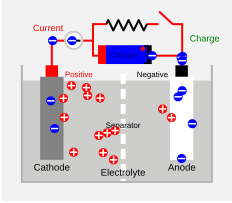
[modifica]Durant la càrrega, el material actiu de l'elèctrode positiu s'oxida, alliberant electrons, i el material de l'elèctrode negatiu és reduït, captant aquests electrons. Aquests electrons constitueixen el flux de corrent elèctric que travessa el circuit extern. L'electròlit pot servir com un simple mitjà de transport per al flux d'ions entre els elèctrodes, com en el cas de la bateria d'ió liti i la bateria de níquel-cadmi, o pot ser un participant actiu en la reacció electroquímica, com en la bateria de plom-àcid.


L'energia utilitzada per carregar les bateries recarregables en la seva majoria prové de corrent altern de la xarxa elèctrica, utilitzant un adaptador (carregador). La majoria dels carregadors de bateries poden trigar diverses hores per carregar una bateria. La majoria de les bateries poden ser carregades en molt menys temps del que fan servir els carregadors de bateries més comuns i simples. Duracell i Rayovac ara venen carregadors que poden regenerar o recarregar bateries de NiMH mida AA i AAA en només 15 minuts; Energizer ven carregadors que poden recarregar bateries de mida C/D i bateries de NiMH de 9 V. No obstant això, les altes taxes de càrrega (per exemple, l'ús de carregadors de 15 minuts o carregadors d'1 hora) causaran dany a llarg termini en les bateries recarregables de NiMH i en la majoria de les altres.
Les bateries recarregables són susceptibles a danys a causa de recàrrega inversa (inversió dels pols) si estan completament descarregades. Hi ha carregadors de bateries totalment integrats que optimitzen el corrent de càrrega.
A més, l'intent de recarregar les piles o bateries no recarregables comporta una petita possibilitat de causar una explosió de la pila.
Les bateries de flux, que no són utilitzades habitualment pels consumidors, es recarreguen mitjançant la substitució del líquid electròlit.
En les especificacions tècniques dels fabricants de la bateria sovint es refereixen al paràmetre VPC. VPC significa volts per cel·la, i es refereix al voltatge de les cel·les individuals que conformen la bateria o cel·la secundària. Per exemple, per carregar una bateria de 12 V (amb 6 cel·les de 2 V cadascuna) a 2,3 VPC es necessita una tensió de 6*(2,3) V = 13,8 V a través dels terminals externs de la bateria.
La majoria de piles de NiMH tipus AA o AAA disposen de cel·les d'1,2 V. Tanmateix, això no és un problema en la majoria dels dispositius perquè les piles alcalines pateixen una caiguda de tensió quan s'esgota l'energia. La majoria dels dispositius estan dissenyats per seguir funcionant amb un voltatge reduït d'entre 0,9 i 1,1 V.
Recàrrega inversa (polaritat invertida)
[modifica]La recàrrega inversa danya les piles, i es produeix quan una bateria recarregable es recarrega amb la polaritat invertida. La recàrrega inversa es pot produir en una sèrie de circumstàncies, essent les tres més comunes les següents:
- Quan la bateria està incorrectament inserida en el carregador, amb els pols al revés.
- Quan un carregador de bateries de tipus automoció està connectat a la inversa als terminals de la bateria. Això sol passar quan es carrega una bateria completament descarregada, en cas contrari es produiran espurnes.
- Quan les cel·les estan connectades en sèrie i molt descarregades.
Quan una cel·la es descarrega completament i no les altres, les cel·les no descarregades s'aplicaran un corrent invers a la cel·la descarregada. Això és comunament anomenat "inversió de la cel·la". La inversió de cel·la escurça significativament la vida de la cel·la afectada, per la qual cosa escurça la vida en general de la bateria. En algunes cel·les de tipus Ni-Cd presenten una efecte memòria.. Algunes cel·les de tipus Ni-Cd, si no es carreguen i descarreguen completament cada cert temps, poden perdre la seva capacitat de mantenir una càrrega completa, és a dir, presenten disminució de la capacitat. Reciclar una bateria multicel·la en descàrrega profunda per superar aquest efecte memòria pot causar reversió de cèl·les i fer més mal que bé. En aplicacions crítiques que utilitzen bateries de Ni-Cd, com en els avions, cada cel·la es descarrega individualment mitjançant la connexió d'un clip de càrrega en els terminals de cada cel·la, evitant així la inversió de cel·la per, a continuació, carregar les piles en sèrie.
Profunditat de descàrrega
[modifica]La profunditat de descàrrega s'estableix normalment com un percentatge de la capacitat nominal en amperes-hora, un 0% de profunditat de descàrrega vol dir que no hi ha descàrrega. Com que la capacitat utilitzable d'una bateria depèn de la velocitat de descàrrega i de la tensió admissible al final de la descàrrega, la profunditat de la descàrrega ha d'estar qualificada per mostrar de quina manera es va a mesurar. A causa de les variacions en la fabricació i l'envelliment de la bateria, la profunditat de descàrrega per a la descàrrega completa pot canviar amb el temps i els cicles de descàrrega. En general, un sistema de bateries recarregable va a tolerar més cicles de càrrega i descàrrega si la profunditat de descàrrega és més baixa en cada cicle.[3]
Components actius
[modifica]Els components actius d'un cel·la secundària són els productes químics que componen els materials actius dels elèctrodes positiu i negatiu, i l'electròlit. Els elèctrodes positiu i negatiu contenen diferents materials: en el positiu es presenten materials amb un potencial de reducció alt o positius, en el negatiu tindrem materials amb potencial d'oxidació baix o negatius. La diferència d'aquests potencials és el potencial estàndard de cel·la o força electromotriu (ε) o tensió de la pila.
En les cèl·lules primàries els elèctrodes positiu i negatiu són coneguts com a càtode i ànode, respectivament. Encara que aquest conveni es trasllada de vegades als sistemes recarregables - especialment les piles d'ions liti, a causa del seu origen en les cel de liti - aquesta pràctica pot portar a confusió. En les piles recarregables l'elèctrode positiu és el càtode en la descàrrega i l'ànode en la càrrega, i viceversa per l'elèctrode negatiu.
Taula de tecnologies usades en les bateries i piles recarregables
[modifica]| Type | Voltatge a | Densitat d'energia b | Potència c | Eficiència d | E/$ i | Descarrega f | Cicles g | Vida mitjana h | ||
|---|---|---|---|---|---|---|---|---|---|---|
| (V) | (MJ/kg) | (Wh/kg) | (Wh/L) | (W/kg) | (%) | (Wh/$) | (%/mes) | (#) | (anys) | |
| Plom i àcid | 02/01 | 0,11-0,14 | 30-40 | 60-75 | 180 | 70% -92% | 5-8 | 3% -4% | 500-800 | 05/08 (bateria de cotxe), 20 (estacionària) |
| Bat. segellades VRLA i | 2.105 | |||||||||
| Alcalina | 01/05 | 0,31 | 85 | 250 | 50 | 99,9% | 07/07 | <0,3 | 100-1000 | <5 |
| Ni-Ferro | 02/01 | 0,18 | 50 | 100 | 65% | 5-7.3[4] | 20% -40% | 50+ | ||
| Ni-Cadmi | 02/01 | 0,14-0,22 | 40-60 | 50-150 | 150 | 70% -90% | 20% | 1500 | ||
| Ni-H 2 | 01/05 | 75 | 20.000 | 15+ | ||||||
| NiMH | 02/01 | 0,11-0,29 | 30-80 | 140-300 | 250-1000 | 66% | 1.37 | 20% | 1000 | |
| Ni-zinc | 01/07 | 0,22 | 60 | 170 | 900 | 2-3.3 | 100-500 | |||
| ió Li | 03/06 | 0,58 | 160 | 270 | 1800 | 99,9% | 2.8-5[5] | 5% -10% | 1200 | 2-3 |
| polímers Li | 03/07 | 0,47-0,72 | 130-200 | 300 | 3000+ | 99,8% | 2.8-5.0 | 500 # 1000 | 2-3 | |
| LiFePO 4 | 25/03 | 80-120 | 170[6] | 1400 | 0.7-3.0 | 2000+[7] | ||||
| Li sofre[8] | 2.0 | 0.94-1.44[9] | 400[10] | 350 | # 100 | |||||
| Li titanat | 02/03 | 90 | 4000+ | 87-95% r | 0.5-1.0[11] | 9000+ | 20+ | |||
| Li pel·lícula prima | ? | 350 | 959 | ? | ? P [12] | 40000 | ||||
| ZnBr | 75-85 | |||||||||
| V redox | 1.15-1.55 | 25-35[13] | 80%[14] | 20%[14] | 14,000[15] | 10 (estacionari)[14] | ||||
| NAS | 150 | 89% -92% | ||||||||
| Sal fosa | 70-110[16] | 150-220 | 4.54[17] | 3000+ | 8+ | |||||
| Plata-zinc (Ag-Zn) | 1.86 | 130 | 240 | |||||||
- Notes
Per comoditat, les entrades a la taula anterior van haver de ser abreujades. Per a una descripció completa, vegeu l'article individual sobre cada tipus de pila o bateria. Els tipus de bateries per als que no hi ha cap article encara s'enumeren a continuació.
- A Tensió nominal de la pila en V.

- B Densitat d'energia = energia/pes o energia/mida, donada en tres diferents unitats.
- C Potència específica = potència/pes en W/kg
- D % eficiència càrrega/descàrrega
- I Quocient Energia/preu al consumidor en W · h/dòlars EUA (Aproximadament)
- J Profunditat de descàrrega de seguretat per mantenir els cicles de vida
- F Velocitat de autodescàrrega en%/mes
- G Durabilitat de cicles, en nombre de cicles.
- H Temps de durada en anys
- I Bateries segellades VRLA o recombinants (inclou bateries amb electròlit fixat en gel i absorbit en feltre).
- P Producció pilot.
- R Depèn de la taxa de càrrega.
Bateries recarregables més comuns
[modifica]- Bateria de níquel-cadmi (NiCd)
- Creada per Waldemar Jungner de Suècia el 1899, basada en la primera bateria alcalina de Thomas Edison. Utilitza òxid hidròxid de níquel i cadmi metàl·lic com elèctrodes. El cadmi és un element tòxic, i va ser prohibit per a la majoria dels usos per la Unió Europea el 2004. Les bateries de níquel-cadmi han estat gairebé completament substituïdes per bateries de níquel-hidrur metàl·lic.
- Bateria de níquel i hidrur metàl·lic (NiMH)
- Es va desenvolupar per primera vegada al voltant de 1980. La bateria té un aliatge capaç d'absorbir hidrogen com elèctrode negatiu, en comptes de cadmi.
- Bateria d'ions de liti
- La tecnologia de la bateria d'ions de liti encara no ha arribat a la maduresa. No obstant això, aquestes bateries són l'elecció preferent en electrònica de consum i moltes tenen una de les millors relacions energia/massa i una pèrdua molt lenta de càrrega quan no està en ús. La popularitat d'aquest tipus de bateries s'ha anat estenent mentre la seva tecnologia continua millorant.
Tipus menys comuns
[modifica]- Bateria de liti-sofre
- Un nou model de bateria desenvolupat per Sion Power des de 1994.[18] Afirma posseir un quocient energia/pes superior que les tecnologies actuals de bateries de liti en el mercat. També el seu menor cost material pot ajudar que aquest producte arribi al mercat de masses.[19] Cal no confondre amb les bateries de diòxid de sofre i liti (Li-SO 2 ) que exploten quan es recarreguen.
- Bateria de pel·lícula prima
- Una millora emergent de la tecnologia d'ions de liti ha estat duta a terme per Excellatron.[20] Els desenvolupadors proclamen haver aconseguit un augment molt gran en els cicles de recàrrega, al voltant de 40.000 cicles. Amb taxes de càrrega i descàrrega. Almenys 5 C de taxa de càrrega. Descàrregues mantingudes de 60 C, i pics de taxa de descàrrega de 1000 C. I també un augment significatiu de l'energia específica, i la densitat d'energia.[21]
També Infinite Power Solutions fabrica bateries de pel·lícula prima (TFB) per aplicació de micro-electrònica, que són piles de liti d'estat sòlid, flexibles i recarregables.[22]
- Bateria intel·ligent
- Una bateria intel·ligent té el circuit de control de la tensió construït a l'interior.
- Bateria de plom i àcid, amb carboni en escuma
- Firefly Energy ha desenvolupat una bateria de plom i àcid, amb carboni en escuma, amb una densitat d'energia reportada d'un 30-40% més que el seu valor original 38 Wh/kg,[23] amb una durada llarga i alta densitat de potència.
Investigacions recents
[modifica]El 2007, el professor ajudant Yi Cui i els seus col·legues del Departament de Ciència i Enginyeria dels Materials, de la Universitat Stanford, van descobrir que, usant nanocables de silici com ànode, s'augmenta la densitat de càrrega volumètrica de l'ànode fins a 10 vegades.[24][25]
Una altra novetat és la invenció de les bateries flexibles, que es poden fer amb paper fi.[26][27]
Ceramatec, una filial de recerca i desenvolupament de CoorsTek, està provant una bateria que conté un tros de metall de sodi sòlid associat a un compost de sofre per una extraordinària membrana de ceràmica fina com el paper. La membrana condueix els ions d'un costat a l'altre i genera un corrent. La companyia afirma que pot posar al voltant de 40 quilowatts-hora d'energia en un paquet de la mida d'un refrigerador, i operar per sota de 90 graus Celsius. L'empresa també afirma que la seva bateria permetrà 3.650 cicles de recàrrega (o aproximadament 1 cop per dia durant una dècada.)[28]
Alternatives
[modifica]Per a usos com ràdios portàtils i llanternes, les bateries recarregables poden ser substituïdes per mecanismes de rellotgeria o dinamos que es mouen amb una maneta per l'usuari per proporcionar l'energia. Per al transport, sistemes de subministrament ininterromput d'energia i laboratoris, els sistemes d'emmagatzematge d'energia mitjançant volant emmagatzemen energia en un rotor que gira per reconversió en energia elèctrica quan sigui necessari; aquests sistemes es poden utilitzar per proporcionar grans polsos d'energia que d'altra manera seria objectable en una xarxa elèctrica comuna.
Un desenvolupament futur podria ser l'ús d'ultracondensadors per al sector del transport, utilitzant un gran condensador per emmagatzemar l'energia en comptes dels bancs de bateries recarregables usats en vehicles híbrids. Un inconvenient dels condensadors en comparació amb les bateries és que la tensió en borns disminueix ràpidament, un condensador que a qui li queda el 25% de la seva energia inicial, tindrà la meitat de la tensió inicial. Els sistemes de bateries tendeixen a tenir una tensió en els terminals que no disminueix ràpidament fins a gairebé estar esgotats. Aquesta característica dificulta el disseny d'electrònica de potència per a l'ús amb ultracapacitador és. Tanmateix, hi ha beneficis potencials en l'eficiència del cicle, la durada, i el pes en comparació amb els sistemes recarregables.
Vegeu també
[modifica]Referències
[modifica]- ↑ David Linden, Thomas B. Reddy (ed). Handbook Of Batteries 3rd Edition. McGraw-Hill, New York, 2002 ISBN 0-07-135978-8 chapter 22
- ↑ Batteries Product Stewardship|Waste|EPA
- ↑ Reddy, Handbook of Batteries pag. 22-20
- ↑ «mpoweruk.com: Accumulator and battery comparisons (pdf)». Arxivat de l'original el 2018-03-29. [Consulta: 17 juliol 2010].
- ↑ http://www.werbos.com/E/WhoKilledElecPJW.htm (que enllaça amb http://www.thunder-sky.com/home_en.asp Arxivat 2007-09-29 a Wayback Machine.)
- ↑ [1]
- ↑ «Zero Emission Vehicles Austràlia». Arxivat de l'original el 2011-12-14. [Consulta: 17 juliol 2010].
- ↑ «Lithium_Sulfur». Arxivat de l'original el 2007-12-14. [Consulta: 17 juliol 2010].
- ↑ [2]
- ↑ http://www.polyplus.com/inproperty/patents/pat6358643.PDF Arxivat 2007-08-01 a Wayback Machine.
- ↑ «Power & Energy Systems FAQ». Arxivat de l'original el 2008-07-04. [Consulta: 17 juliol 2010].
- ↑ «Excellatron». Arxivat de l'original el 2012-08-08. [Consulta: 17 juliol 2010].
- ↑ Redox Battery[Enllaç no actiu]
- ↑ 14,0 14,1 14,2 «Còpia arxivada». Arxivat de l'original el 2016-05-17. [Consulta: 17 juliol 2010].
- ↑ «The Vanadium Advantage: Flow Batteries Put Wind Energy in the Bank». Arxivat de l'original el 2008-09-07. [Consulta: 17 juliol 2010].
- ↑ http://www.betard.co.uk/new_zebra.pdf Arxivat 2007-09-28 a Wayback Machine.
- ↑ «EVWORLD Feature: Fuel Cell disruptor - Part 2: BROOKS FUEL CELL|CARB|ARB|Hydrogen|ZEBRA|EV|ELECTRIC». Arxivat de l'original el 2012-05-25. [Consulta: 17 juliol 2010].
- ↑ Sion Power Corporation - Advanced Energy Storage: Welcome
- ↑ «Sion Power Corporation - Advanced Energy Storage: Technology Overview». Arxivat de l'original el 2012-11-10. [Consulta: 17 juliol 2010].
- ↑ Excellatron
- ↑ «Excellatron - the Company». Arxivat de l'original el 2012-09-12. [Consulta: 17 juliol 2010].
- ↑ http://www.infinitepowersolutions.com/
- ↑ com/2008/01/firefly-energy.html Green Car Congress: Firefly Energy Eyeing the Hybrid Market; Lead-Acid Foam Batteries for Mild-Hybrid Applications Heading to DOE for Testing and Validation [Enllaç no actiu]
- ↑ Serpa, Alex. A tenfold improvement in battery life?. CNET, 15 gener 2008 [Consulta: 12 abril 2008].[Enllaç no actiu]
- ↑ «High-performance Lithium battery ànodes using Silicon nanowires». Nanotechnology 3, 31 - 35 (2008). Nature, 16-12-2007. DOI: 10.1038/nnano.2007.411.
- ↑ «Self pila battery (flexible organic battery)». Arxivat de l'original el 2009-07-14. [Consulta: 17 juliol 2010].
- ↑ «Power Paper thin and flexible batteries». Arxivat de l'original el 2009-06-26. [Consulta: 17 juliol 2010].
- ↑ html New battery could change the world, one house at a time[Enllaç no actiu]

