Enllaç C-Al
Els compostos d'organoalumini (o compostos orgànics de l'alumini) són compostos químics que contenen un enllaç químic entre carboni (C) i alumini (Al) (enllaç C-Al). La química de l'organoalumini és la ciència corresponent que explora les propietats, l'estructura i la reactivitat d'aquests compostos. És un dels temes principals dins de la química organometàl·lica.[1][2]
-
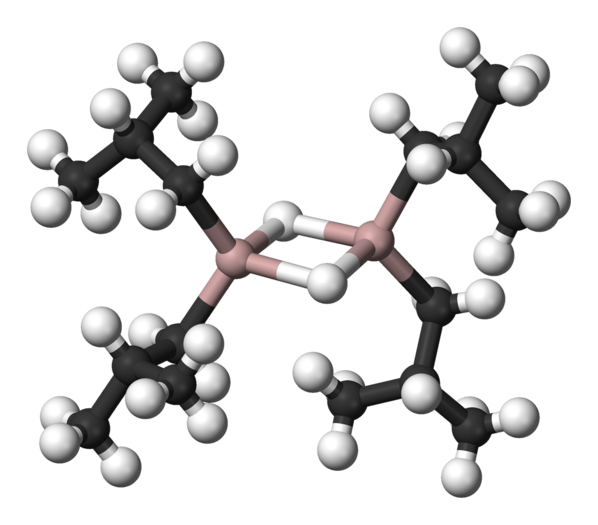
El model de barres i boles d'hidrur de diisobutilalumini, que mostra l'alumini com a rosa, el carboni com a negre i l'hidrogen com a blanc
Els compostos d'organoalumini il·lustratius són el dímer trimetilalumini Al₂(CH₃)₆, el monòmer triisobutilalumini Al(CH₂CH(CH₃)₂)3, i el compost titani-alumini anomenat reactiu de Tebbe (C₅H₅)₂TiCH₂ClAl(CH₃)₂. El comportament dels compostos d'organoalumini es pot entendre en termes de polaritat de l'enllaç C-Al i l'alta acidesa de Lewis de les espècies de tres coordinacions. Industrialment, aquests compostos s'utilitzen principalment per a la producció de poliolefines.
Història
[modifica]El primer compost organoalumini (C₂H₅)₃Al₂I₃ es va descobrir el 1859.[3]
Però els compostos d'organoalumini van ser poc coneguts fins a la dècada del 1950, quan Karl Ziegler i els seus col·legues van descobrir la síntesi directa de compostos de trialquilalumini i van aplicar aquests compostos a la polimerització catalítica d'olefines. Aquesta línia d'investigació finalment va donar lloc al Premi Nobel a Ziegler.
Estructura i enllaç
[modifica]Compostos d'alumini(III)
[modifica]Els compostos d'organoalumini generalment presenten centres d'alumini amb nombre de coordinació 3 i 4, tot i que s'observen nombres de coordinació més alts amb lligands inorgànics com el fluor. D'acord amb les tendències habituals, l'alumini amb nombre de coordinació 4 prefereix ser tetraèdric. A diferència del bor, l'alumini és un àtom més gran i acomoda fàcilment quatre lligands de carboni. Així, els compostos de triorganoalumini solen ser dimèrics amb un parell de lligands de pont alquil, per exemple, Al₂(C₂H₅)₄(μ-C₂H₅)₂. Així, malgrat el seu nom comú de trietilalumini, aquest compost conté dos centres d'alumini i sis grups etil. Quan el compost d'organoalumini conté hidrur o halogenur, aquests lligands més petits tendeixen a ocupar els llocs de pont. La coordinació 3 es produeix quan els grups R són voluminosos, per exemple, Al(Mes)₃ (Mes = 2,4,6-Me₃C₆H₂ o mesitil) o isobutil.[4]
-
Estructura de trimetilalumini, un compost que presenta carbonis amb cinc enllaços
Intercanvi de lligands en compostos de trialquilalumini
[modifica]Els dímers de trialquilalumini sovint participen en equilibris dinàmics, donant lloc a l'intercanvi de lligands de pont i terminals, així com a l'intercanvi de lligands entre dímers. Fins i tot en dissolvents no coordinants, l'intercanvi d'Al-Me és ràpid, tal com confirma l'espectroscòpia de ressonància magnètica nuclear de protons (RMN). Per exemple, a -25 °C, l'espectre de RMN 1H de Me₆Al₂ inclou dos senyals en una proporció 1:2, com s'esperava de l'estructura d'estat sòlid. A 20 °C, només s'observa un senyal perquè l'intercanvi de grups metil terminals i ponts és massa ràpid per ser resolt per RMN.[5] L'elevada acidesa de Lewis de l'espècie monomèrica està relacionada amb la mida del centre d'Al(III) i la seva tendència a aconseguir una configuració d'octet.
El baix estat d'oxidació dels compostos d'organoalumini
[modifica]El primer compost d'organoalumini amb un enllaç Al-Al es va informar el 1988 com (((Me₃Si)₂CH)₂Al)₂ (un dialà). Normalment es preparen reducció dels clorurs de dialquilalumini per potassi metàl·lic:[6]
- (R₂AlCl)₂ + 2 K → R₂Al-AlR₂ + 2 KCl
Un altre grup notable d'alans són els tetraalans que contenen quatre centres Al(I). Aquests compostos adopten un nucli tetraedre, tal com il·lustra (Cp*Al)₄ i ((Me₃Si₃C)Al)₄. El clúster [Al₁₂(i-Bu)₁₂]2− es va obtenir a partir d'investigacions relacionades sobre la reducció de compostos organoalumini. Aquest dianió adopta una estructura icosaèdrica que recorda el dodecaborat ([B₁₂H₁₂]2−). El seu estat d'oxidació formal és inferior a 1.
Preparació
[modifica]A partir d'halogenurs d'alquil i d'alumini
[modifica]Industrialment, els alquils d'alumini simples del tipus Al₂R₆ (R = Me, Et) es preparen en un procés de dues etapes que comença amb l'alquilació de la pols d'alumini:
- 2 Al + 3 CH₃CH₂Cl → (CH₃CH₂)₃Al₂Cl₃
La reacció s'assembla a la síntesi amb reactius de Grignard. El producte, (CH₃CH₂)₃Al₂Cl₃, s'anomena sesquiclorur d'etilalumini. El terme sesquiclorur fa referència al fet que, de mitjana, la relació Cl:Al és d'1,5. Aquests sesquiclorurs es poden convertir en derivats de triorganoalumini per reducció:
- 2 (CH₃CH₂)₃Al₂Cl₃ + 6 Na → (CH₃CH₂)₆Al₂ + 2 Al + 6 NaCl
Aquest mètode s'utilitza per a la producció de trimetilalumini i trietilalumini.[7]
Hidroaluminació
[modifica]La pols d'alumini reacciona directament amb certs alquens terminals en presència d'hidrogen. El procés consta de dues etapes, la primera produint hidrurs de dialquilalumini. Aquestes reaccions es duen a terme normalment a temperatures elevades i requereixen activació mitjançant reactius de trialquilalumini:
- 6 Al + 3 H₂ + 12 CH₂=CHR → 2 [HAl(CH₂CHR)₂]₃
Per als grups R no voluminosos, els hidrurs d'organoalumini solen ser trimèrics. En un pas posterior, aquests hidrurs es tracten amb més alquè per efectuar la hidroaluminació:
- 2 [HAl(CH₂CHR)₂]₃ + 3 CH₂=CHR → 3 [Al₂(CH₂CHR)₃
L'hidrur de diisobutilalumini, que és dimèric, es prepara mitjançant l'eliminació d'hidrur del triisobutilalumini:
- 2 i-Bu₃Al → (i-Bu₂AlH)₂ + 2 (CH₃)₂C=CH₂
Carboaluminació
[modifica]Els compostos d'organoalumini poden reaccionar amb alquens i alquins, donant lloc a l'addició neta d'un grup orgànic i el fragment metàl·lic a través de l'enllaç múltiple (carboaluminació). Aquest procés pot procedir d'una manera purament tèrmica o en presència d'un catalitzador de metalls de transició. Per al procés no catalitzat, la monoaddició només és possible quan es substitueix l'alquè. Per a l'etilè, la carboaluminació condueix a una distribució de Poisson d'espècies d'alquilalumini superiors. La reacció és regioselectiva per als 1-alquens.[8] L'anomenada reacció ZACA, informada per primera vegada per Ei-ichi Negishi, és un exemple d'una carboaluminació asimètrica d'alquens catalitzada per un catalitzador de zirconocè quiral.[9]
La metilaluminació d'alquins en presència de Cp₂ZrCl₂[10][11] s'utilitza per a la síntesi de fragments d'olefines trisubstituïdes estereodefinides, una subestructura comuna en productes naturals de terpens i policètids. La síntesi de (E)-4-iodo-3-metilbut-3-en-1-ol[12] que es mostra a continuació és una aplicació típica d'aquesta reacció:
-
Carboaluminació
Per als alquins terminals, la reacció generalment transcorre amb una bona regioselectivitat (>90:10 rr) i una selectivitat sin completa, fins i tot en presència de substituents d'heteroàtom propargílics o homopropargílics. Malauradament, l'extensió de la metilaluminació catalitzada per zirconocè a l'alquilaluminació amb alquils més alts dona lloc a rendiments més baixos i regioselectivitats pobres.
Preparacions al laboratori
[modifica]Tot i que els membres simples estan disponibles comercialment a baix cost, s'han desenvolupat molts mètodes per a la seva síntesi al laboratori, incloent metàtesi o transmetal·lació. La metàtesi del triclorur d'alumini amb RLi o RMgX dona el trialquil:
- AlCl₃ + 3 BuLi → Bu₃Al + 3 LiCl
- Transmetal·lació:
- 2 Al + 3 HgPh₂ → 2 AlPh₃ + 3 Hg
Reacció
[modifica]L'alta reactivitat dels compostos d'organoalumini cap als electròfils s'atribueix a la separació de càrrega entre l'alumini i l'àtom de carboni.
Acidesa de Lewis
[modifica]Els compostos d'organoalumini són àcids durs i formen fàcilment adductes amb bases com la piridina, el THF i les amines terciàries. Aquests adductes són tetraèdrics a Al.
Electròfils
[modifica]L'enllaç Al-C està polaritzat de manera que el carboni és molt bàsic. Els àcids reaccionen per donar alcans. Per exemple, els alcohols donen alcòxids:
- AlR'₃ + ROH → 1/n (R'₂Al−OR)n + R'H
Es pot utilitzar una àmplia varietat d'àcids més enllà dels àcids minerals simples. Les amines donen derivats d'amido. Amb el diòxid de carboni, els compostos de trialquilalumini donen el carboxilat de dialquilalumini i, posteriorment, els dicarboxilats d'alquilalumini:
- AlR₃ + CO₂ → R₂AlO₂CR
- R₂AlO₂CR + CO₂ → RAl(O₂CR)₂
La conversió recorda la carbonació dels reactius de Grignard.[13][14]
De la mateixa manera, la reacció entre compostos de trialquilalumini i diòxid de carboni s'ha utilitzat per sintetitzar alcohols, olefines[13] o cetones.[15]
Amb l'oxigen s'obtenen els alcòxids corresponents, que es poden hidrolitzar a alcohols:
- AlR₃ + 3/2 O₂ → Al(OR)₃
Un peròxid d'organoalumini caracteritzat estructuralment és [{HC[C(Me)N-C₆H₅]₂}Al(R)-O-O-CMe₃] [R=CH(SiMe₃)₂].[16]
La reacció entre compostos de trialalquilalumini pur amb aigua, alcohols, fenols, amines, diòxid de carboni, òxids de sofre, òxids de nitrogen, halògens i hidrocarburs halogenats pot ser violenta.[17][18]
Polimerització d'alquens
[modifica]Industrialment, els compostos d'organoalumini s'utilitzen com a catalitzadors per a la polimerització d'alquens a poliolefines, per exemple el catalitzador metilaluminoxà.
Referències
[modifica]- ↑ Shriver i Atkins, 2006.
- ↑ Witt i Roesky, 2000, p. 410.
- ↑ Hallwachs i Schafarik, 1859, p. 206-209.
- ↑ Elschenbroich, 2006.
- ↑ Cotton i Wilkinson, 1980, p. 343.
- ↑ Uhl, 2004, p. 53-108.
- ↑ Krause et al., 2005.
- ↑ Trost, Semmelhack i Fleming, 1992.
- ↑ Negishi, 2011, p. 34-53.
- ↑ Negishi, Ei-ichi; Wang, Guangwei; Rao, Honghua; Xu, Zhaoqing «Alkyne Elementometalation−Pd-Catalyzed Cross-Coupling. Toward Synthesis of All Conceivable Types of Acyclic Alkenes in High Yields, Efficiently, Selectively, Economically, and Safely: "Green" Way» (en anglès). The Journal of Organic Chemistry, 75(10), 14-05-2010, pàg. 3151–3182. DOI: 10.1021/jo1003218. PMC: 2933819. PMID: 20465291.
- ↑ Negishi, 2002, p. 963-975.
- ↑ Rand, Cynthia L.; Horn, David E. Van; Moore, Mark W.; Negishi, Eiichi «A versatile and selective route to difunctional trisubstituted (E)-alkene synthons via zirconium-catalyzed carboalumination of alkynes» (en anglès). The Journal of Organic Chemistry, 46(20), 01-05-2002, pàg. 4093–4096. DOI: 10.1021/jo00333a041.
- ↑ 13,0 13,1 Yur'ev, Kuchin i Tolstikov, 1974, p. 817-819.
- ↑ Ziegler, 1956, p. 721-729.
- ↑ David W. Marshall, US patent US3168570, assignat a Continental Oil. (anglès)
- ↑ Uhl i Jana, 2008, p. 3067-3071.
- ↑ Cameo Chemicals SDS
- ↑ Handling Chemicals Safely 1980. p. 929
Bibliografia
[modifica]- Cotton, Frank Albert; Wilkinson, Geoffrey. Advanced Inorganic Chemistry (en anglès), 1980. ISBN 978-0-471-02775-1.
- Elschenbroich, C. Organometallics (en anglès). Weinheim: Wiley-VCH, 2006. ISBN 978-3-527-29390-2.
- Hallwachs, W.; Schafarik, A. «Ueber die Verbindungen der Erdmetalle mit organischen Radicalen» (en alemany). Liebigs Ann. Chem., 109(2), 1859. DOI: 10.1002/jlac.18591090214.
- Krause, Michael J.; Orlandi, Frank; Saurage, Alfred T.; Zietz, Joseph R. «Aluminum Compounds, Organic». A: Ullmann's Encyclopedia of Industrial Chemistry (en anglès). Weinheim: Wiley-VCH, 2005. DOI 10.1002/14356007.a01_543.
- Negishi, Ei-ichi. Organometallics In Synthesis: A Manual (Ed. M. Schlosser) (en anglès). Chichester, West Sussex, UK: Wiley, 2002. ISBN 978-0471984160.
- Negishi, Ei-ichi «Discovery of ZACA reaction : Zr-catalyzed asymmetric carboalumination of alkenes» (en anglès). Arkivoc, 2011(viii), 2011. DOI: 10.3998/ark.5550190.0012.803.
- Shriver, D. F.; Atkins, P. W.. Inorganic Chemistry (en anglès). Oxford University Press, 2006. ISBN 978-0199264636.
- Trost, Barry M.; Semmelhack, Martin F.; Fleming, Ian. Comprehensive Organic Synthesis: Additions to and substitutions at C-C[pi]-Bonds (en anglès). Pergamon, 1992. ISBN 9780080405957.
- Uhl, W. Organoelement Compounds Possessing Al---Al, Ga---Ga, In---In, and Tl---Tl Single Bonds (en anglès). 51, 2004 (Advances in Organometallic Chemistry). DOI 10.1016/S0065-3055(03)51002-4. ISBN 9780120311514.
- Uhl, W.; Jana, B. «A persistent alkylaluminum peroxide: Surprising stability of a molecule with strong reducing and oxidizing functions in close proximity» (en anglès). Chem. Eur. J., 14(1o), 2008. DOI: 10.1002/chem.200701916. PMID: 18283706.
- Witt, M.; Roesky, H. W. «Organoaluminum chemistry at the forefront of research and development» (
 PDF) (en anglès). Curr. Sci., 78(4), 2000. Arxivat de l'original el 2014-10-06 [Consulta: 23 juliol 2022].
PDF) (en anglès). Curr. Sci., 78(4), 2000. Arxivat de l'original el 2014-10-06 [Consulta: 23 juliol 2022]. - Yur'ev, V.P.; Kuchin, A.V.; Tolstikov, G.A. «Reaction of aluminum trialkyls with carbon dioxide» (en anglès). Organic and Biological Chemistry, 23(4), 1974. DOI: 10.1007/BF00923507.
- Ziegler, K. «Neue Entwicklungen der metallorganischen Synthese» (en alemany). Angew. Chem., 68(23), 1956. DOI: 10.1002/ange.19560682302.