Ferrocè
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 186,013 Da |
| Data de descobriment o invenció | 1951 |
| Estructura química | |
| Fórmula química | C₁₀H₁₀Fe |
 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Punt de fusió | 173 ℃ |
| Punt d'ebullició | 249 ℃ (a 760 Torr) |
| Perill | |
| Límit d'exposició mitjana ponderada en el temps | 5 mg/m³ (10 h, Estats Units d'Amèrica) 10 mg/m³ (10 h, cap valor) 15 mg/m³ (8 h, Estats Units d'Amèrica) |
| Altres | |
| sòlid inflamable | |
El ferrocè o ferrocé[a] és un compost organometàl·lic la fórmula molecular del qual és (C₅H₅)₂Fe. Va ser el primer metal·locè sintetitzat que consta d'un centre metàl·lic situat entre dos anells d'anió ciclopentadienil conferint-li literalment una conformació tipus "sandvitx". El descobriment d'aquest nou tipus de compost metal·locè va marcar un abans i un després a la química organometàl·lica.
Història
[modifica]Vora els anys 50 dos grups d'investigació independents van sintetitzar el mateix producte per casualitat mentre treballaven en diferents camps de la química. El primer d'ells (Kealy i Pauson, desembre del 1951) estava intentant obtenir fulvalè a partir del bromur de ciclopentadienilmagnesi i triclorur de ferro. Per contra van obtenir uns cristalls de color ocre ataronjat l'anàlisi elemental dels quals va ser el que es mostra la figura 1.1.[1] El segon investigador (S.A. Miller, gener del 1952) estava treballant en la síntesi d'amoníac (procés de Haber-Bosch), i va obtenir el mateix compost per reacció directa del ciclopentadiè amb ferro, en presència d'òxids d'alumini, potassi o molibdè a 300 °C. Van publicar els resultats el 1952, tot i que el descobriment l'havien fet tres anys abans.[2] Tots dos grups d'investigació coincidien en el fet que el producte obtingut era estable a l'aire, podia sublimar-se, amb un punt de fusió de 173 °C, molt soluble en dissolvents orgànics però insoluble en aigua.
Primer grup d'investigació: Kealy i Pauson
[modifica]

Segon grup d'investigació: S.A. Miller
[modifica]C5H6 + Fe → (C5H5)2Fe + H2
Estructura i enllaç químic
[modifica]
La primera estructura proposada pel ferrocè consistia en dos anells de ciclopentadienils plans units a un àtom central de ferro destacant el caràcter covalent de l'enllaç.(figura 1.2.) Aquesta estructura va presentar un enorme interès i ràpidament es va intentar resoldre. En primer lloc, hi havia alguns fets que no podien ser explicats considerant dos enllaços sigma en el compost; per exemple, les propietats tèrmiques i les químiques. A més a més, l'enllaç sigma entre l'àtom metàl·lic i els ciclopentadienils hauria de ser relativament inestable i la volatilitat no podria ser conseqüència d'una interacció iònica.
Seguidament, Wilkinson i Woodward – a la Universitat Harvard- van utilitzar mètodes físics i espectroscòpics per determinar l'estructura correcta del ferrocè mentre que simultàniament i de manera independent, Fisher i Pfab usaven la cristal·lografia de raigs X sobre el monocristall.
Wilkinson advertí que els deu àtoms de carboni havien de contribuir de la mateixa manera a l'enllaç amb el ferro. Per això va deduir que l'estructura havia de consistir en dos anells ciclopentadienils paral·lels i l'àtom de ferro al centre d'aquests com si fos un "sandvitx".(figura 1.3.)

Així, l'enllaç havia de ser molt fort a causa de la superposició dels orbitals del metall i els electrons ∏ dels orbitals del ciclopentadienil. Per comprovar aquesta hipòtesi, es van fer estudis d'RI, de RMN, UV-VIS, mesures del moment dipolar, arribant a la conclusió que existia un únic tipus d'enllaç C-H, que el compost era diamagnètic, sense electrons desaparellats, i que el moment dipolar efectiu era zero. Tots aquests fets van indicar que efectivament l'estructura havia de ser del tipus "sandvitx".[3][4][5][6] Uns mesos més tard els estudis cristal·logràfics de Fisher van demostrar l'estructura anteriorment proposada.[7]
El descobriment i reconeixement d'aquest nou tipus d'enllaç entre fragments orgànics insaturats i metalls va marcar l'inici de la química organometàl·lica. El 1973 Fischer professor de la Universitat Tècnica de Múnic i Wilkinson de la Universitat de Londres van compartir el premi Nobel pel seu treball.[14][8]
Síntesi
[modifica]El ferrocè es pot preparar de diverses maneres. Cal destacar que és un compost relativament barat, que es fabrica comercialment, fàcil d'aïllar en forma cristal·lina mitjançant recristal·litzacions, molt soluble en dissolvents orgànics, insoluble en aigua i estable a l'aire. Les formes d'obtenció més habituals són:
- Transmetal·lació
- A partir d'una font de ciclopentadienur[9]
- 2Na(C5H5) + FeCl2 → (C5H5)2Fe + 2NaCl
- Síntesi Directa
- A partir de ferro metàl·lic[10]
- Fe + 2C5H6 ---(500 °C)-→ (C5H5)2Fe
Propietats
[modifica]Propietats electroquímiques
[modifica]
El ferrocè es pot oxidar fàcilment per a donar ferroceni (catió diciclopentadienilferro(III)) de color verd blavós en dissolucions diluïdes o vermell sang en dissolucions concentrades. (esquema 3.1.)
Les sals de ferroceni són molt emprades com a agents oxidants suaus d'un electró i el parell redox ferrocè/ferroceni s'utilitza com un estàndard secundari en molts estudis electroquímics. Això ha portat la incorporació del ferrocè en molts sistemes perquè actuï com interruptor o receptor molecular. En alguns sistemes, el ferrocè pot oferir la possibilitat de la seva aplicació en el camp dels sensors químics i l'electrònica molecular.
Propietats estructurals
[modifica]
Els primers estudis estructurals del ferrocè indicaven que, a temperatura ambient, cristal·litza en el sistema monocíclic adoptant una conformació alternada i amb una simetria molecular. Posteriorment, es va veure que aquesta estructura no era correcta i que el ferrocè presentava polimorfisme. A una temperatura inferior a 164K, el ferrocè cristal·litza en el sistema tricíclic amb una conformació pseudoeclipsada, desviada d=9° (vegeu Figura 3.2.). Per sota de 110 K, la cristal·lització del ferrocè és ortoròmbica amb una conformació totalment eclipsada i de simetria molecular.
Quiralitat del ferrocè
[modifica]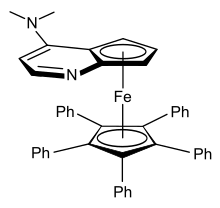
El comportament del ferrocè referent a la seva reactivitat és molt similar al dels sistemes aromàtics. Això no obstant, la estreoquímica del ferrocè és molt diferent. En concret, els derivats del ferrocè amb almenys dos substituents diferents en el mateix anell no són superposables amb la seva imatge especular; és a dir, són quirals. El primer compost d'aquest tipus que es va sintetitzar va ser l'àcid 3,1'-dimetilferrocencarboxílic el 1962. La figura 3.3 mostra un exemple d'estructura quiral derivada del ferrocè.
Reactivitat
[modifica]Una de les característiques fonamentals del ferrocè és que es comporta com un sistema aromàtic degut a l'aromaticitat que li proporcionen els anells ciclopentadienils. D'aquesta manera, la química orgànica del ferrocè es basa i es pot predir en termes d'aromaticitat, sobretot la important substitució aromàtica electròfila. Al següent esquema (esquema 3.4.) es mostren algunes reaccions orgàniques més significatives:

Aplicacions
[modifica]La importància del ferrocè i dels seus derivats resideix en la gran quantitat d'aplicacions que tenen. L'estabilitat, les seves propietats físiques i químiques li proporcionen unes característiques especials que el fan molt útil en moltes àrees de la química. De les múltiples aplicacions en destacarem les més rellevants, com per exemple en el camp de la medicina, la catàlisi i l'anàlisi simètrica.
Polímers amb ferrocè
[modifica]Dins del camp dels materials polimèrics estan adquirint una gran importància els polímers que contenen metalls en la seva estructura, a causa de les propietats que presenten en comparació amb els anàlegs polímers orgànics tradicionals. Com a exemple, cal destacar la conductivitat elèctrica (superconductivitat), el comportament magnètic, l'augment de l'estabilitat tèrmica, propietats ignífugues i les característiques òptiques com els efectes de l'òptica no lineal (ONL). En particular, l'estabilitat i el comportament redox del ferrocè i els seus derivats han produït la seva incorporació en moltes estructures polimèriques. La síntesi d'aquests polímers es basa fonamentalment en dues metodologies:
- a partir de la funcionalització dels polímers orgànics tradicionals, de manera que sigui fàcil la introducció del fragment metàl·lic
- a partir de la introducció de fragments polimeritzables en els derivats metàl·lics
Un dels primers exemples d'aquesta síntesi va ser el vinilferrocilè per a donar polivinilferroceni.[11] El ferrocè és un compost que presenta propietats ingnífugues importants, d'aquí que hagi estat utilitzat per a l'obtenció de materials polimèrics ignífugs. Existeixen molts tipus de polímers derivats del ferrocè, com poden ser els polímers quirals, els units cara a cara, els polímers tridimensionals i els dendrímers. En general, els polímers lineals de ferrocè tenen la fórmula que mostra la figura 3.5.

X és un halur o un hidròxid R és un grup d'èster d'aproximadament 10 àtoms de carbonis Z és el liti, l'hidrogen o un grup de la fórmula
Un altre exemple de reacció polimèrica amb el ferrocè és la reacció de ferrocè amb fenildihalofosfines. Els productes (figura 3.6.) tenen la següent fórmula estructural:

Sals de transferència: materials conductors i magnètics
[modifica]El descobriment, a la dècada dels vuitanta, de materials moleculars amb propietats tradicionalment relacionades amb els metalls, com la superconductiviat i el magnetisme ha estimulat l'interès científic en aquesta àrea de coneixement. Els materials moleculars solen ser lleugers, transparents i presenten propietats òptiques. La base molecular d'un compost de transferència de càrrega (TC) consisteix en un donador i un acceptor de densitat electrònica, capaços de formar cations i anions radicals (electròfil, nucleòfil), i en estat sòlid, aquests compostos han de presentar una adequada manera d'apilar-se perquè es pugui produir la conducció elèctrica. Els complexos de TC han de complir certs requisits per a presentar un determinat apilament en estat sòlid:
- Les molècules han de ser planes o estar compostes per fragments que ho siguin.
- Han de formar radicals estables en la dissolució en els que la diferència energètica entre els orbitals HOMO i LUMO sigui relativament petita.
- Han de presentar sistemes conjugats i han de ser capaces d'aproximar-se unes a les altres més a prop que la suma de la distància de radis de Van der Waals, augmentant d'aquesta manera la superposició intermolecular.
El ferrocè és una molècula cilíndrica compacta amb dos anells plans paral·lels. A més a més, és fàcilment oxidable per a donar sals estables de ferroceni, i la seva capacitat donadora pot ser modificada amb el número i la naturalesa dels substituents. El ferrocè forma complexos de TC febles, això no obstant, el decametilferrocè forma complexos molt més interessants. La introducció de metils produeix que el compost sigui molt més fàcil d'oxidar i més resistent a reaccions de substitució. L'any 1979 es va descobrir que el compost [CpFe(III)][TCNQ] tenia un elevat moment ferromagnètic i una estructura lineal. A partir d'aquí, es van fer molts estudis per tal d'estabilitzar el ferromagnetisme.
Derivats del ferrocè en medicina
[modifica]
Biosensors
[modifica]Un dels biosensors més importants és el corresponent a la glucosa. No només pel seu ús en processos biotecnològics com el control de processos de fermentació, sinó també en el camp de la medicina. S'usa, per exemple, per a mesurar la glucosa en sang en el diagnòstic de l'estat de la diabetis mellitus i la hiperglucèmia. L'oxidació de la glucosa per l'enzim oxidasa (GOD) per a formar el glutanat és sensible i específica i, d'aquesta manera, apropiada per a la determinació de glucosa amb sensors. El resultat de la reacció bioquímica entre l'enzim i la glucosa pot ser avaluat a través de l'oxigen consumit o del peròxid d'hidrogen format. Això no obstant, la mesura electroquímica directa del producte oxidat està impedida perquè l'enzim no reacciona amb les superfícies de l'elèctrode directament i també allà pot ser dissolt l'oxigen de les mostres. Així, es pot usar un mediador redox per facilitar l'oxidació de la glucosa en condicions catalítiques. Per oxidació de la forma reduïda del GOD es pot saber la quantitat de glucosa transformada en gluconat. El parell ferrocè/ferroceni pot actuar com a mediador permetin la determinació electroquímica de la glucosa a través d'uns cicles electroquímics encadenats, com mostra la figura 3.9.

Agents antitumorals
[modifica]

Hi ha un compost molt conegut en el tractament contra el càncer conegut amb el nom de cisplatí. El principal inconvenient del compost, però, és que presenta alguns efectes col·laterals adversos. Avui dia els estudis se centren en la recerca de compostos altament eficaços i que siguin menys tòxics.
Alguns derivats del ferrocè han demostrat propietats antitumorals molt bones, com per exemple el ferroceni. Les sals derivades de ferroceni solubles en aigua són agents eficaços en el tractament del tumor Erlich Ascites, arribant a uns nivells de cura d'entre el 70% i el 100%. Altres tumors inhibits pel ferroceni són el melanoma B16, carcinoma de còlon 38 i el carcinoma de pulmó de Lewis. El principal avantatge d'ús d'aquests compostos és que són molt menys tòxics que els derivats de platí.
Referències
[modifica]- ↑ Kealy, T. J.; Pauson, P. L. «"A New Type of Organo-Iron Compound"». Nature, 168 (4285), 1951, pàg. 1039. DOI: 10.1038/1681039b0.
- ↑ Miller, S. A., Tebboth, J. A., Tremaine, J. F. «"114. Dicyclopentadienyliron"». Journal of the Chemical Society, 1952, pàg. 632–635. DOI: 10.1039/JR9520000632.
- ↑ Pierre Laszlo, Roald Hoffmann, «"Ferrocene: Ironclad History or Rashomon Tale?"». Angewandte Chemie International Edition, nº 39 (1), 2000, pàg. 123–124. DOI: 10.1002/(SICI)1521-3773(20000103)39:1<123::AID-ANIE123>3.0.CO;2-Z. PMID: 10649350.
- ↑ Werner, H. «"At Least 60 Years of Ferrocene: The Discovery and Rediscovery of the Sandwich Complexes"». Angew. Chem. Int. Ed., nº51, 2012, pàg. 6052–6058. DOI: 0.1002/anie.201201598.
- ↑ Dunitz, J. D., Orgel, L. E. «"Bis-Cyclopentadienyl – A Molecular Sandwich"». Nature, nº171 (4342), 1953, pàg. 121–122. DOI: 10.1038/171121a0.
- ↑ P. F. Eiland and R. Pepinsky «"X-ray examination of iron biscyclopentadienyl"». Journal of the American Chemical Society, nº 74 (19), 1952, pàg. 4971. DOI: 10.1021/ja01139a527.
- ↑ J. Dunitz, L. Orgel, A. Rich «"The crystal structure of ferrocene"». Acta Crystallographica, nº9 (4), 1956, pàg. 373–375. DOI: 10.1107/S0365110X56001091.
- ↑ Pàgina oficial de l'Acdèmia Reial de Ciències Sueca, premis Nobel 1973
- ↑ 9,0 9,1 Geoffrey Wilkinson «"Ferrocene"». Organic Syntheses, 4, 1963, pàg. 473.
- ↑ Wilkinson, G.; Cotton, F. A.; Birmingham, J. M. «"On manganese cyclopentadienide and some chemical reactions of neutral bis-cyclopentadienyl metal compounds"». J. Inorg. Nucl. Chem., nº 2 (2), 1956, pàg. 95. DOI: 10.1016/0022-1902(56)80004-3.
- ↑ Liu, Wan-yi; Xu, Qi-hai; Ma, Yong-xiang; Liang, Yong-min; Dong, Ning-li; Guan, De-peng «"Solvent-free synthesis of ferrocenylethene derivatives"». J. Organomet. Chem., nº 625, 2001, pàg. 128–132. DOI: 10.1016/S0022-328X(00)00927-X.
Notes
[modifica]- ↑ Ferrocé segons la pronúncia occidental i la normativa valenciana, i ferrocè segons la pronúncia oriental. Per a més informació, consulteu el Llibre d'estil.
