Peptidil transferasa
| Identificadors | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Número EC | 2.3.2.12 | ||||||||
| Bases de dades | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | metabolic pathway | ||||||||
| PRIAM | profile | ||||||||
| Estructures PDB | RCSB PDB PDBj PDBe PDBsum | ||||||||
| |||||||||
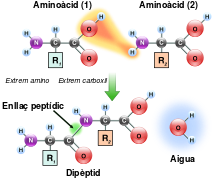
L'enzim peptidil transferasa és una aminoacil transferasa (amb nombre EC 2.3.2.12) que realitza la funció essencial de les ribosomes. S'encarrega de la formació d'enllaços peptídics entre aminoàcids adjacents durant la traducció de l'ARN missatger i, per tant, la síntesi proteica; l'energia per fer-ho l'obté de trencar la unió aminocil-ARNt.
No obstant això, aquests enzims estan implicats també en processos no relacionats amb la traducció. En bacteris, l'activitat peptidil transferasa es troba en la subunitat 50 S (component 23 S); en canvi, en eucariotes són la subunitat 60 S (component 28 S) la que l'allotja.
Ús terapèutic
[modifica]
Diversos quimioteràpics posseeixen la seva diana en l'activitat peptidil transferasa, com a element crucial en la síntesi proteica. Depenent de la seva afinitat per ribosomes procariotes o eucariotes, s'empren en teràpia antimicrobiana específica (els primers, contra bacteris; els segons, contra fongs, fonamentalment)
- El cloramfenicol uneix l'ARN ribosomal 23 S als seus residus A2451 i A2452, inhibint la formació de l'enllaç peptídic.[1] És actiu davant un ampli espectre de microorganismes, en especial estafilococs.
- Els antibiòtics macròlids sembla inhibir a la peptidil transferasa durant el pas de translocació ribosomal.[2] Entre ells es troben fàrmacs antibacterians com l'eritromicina.
- La cicloheximida és un inhibidor de la síntesi proteica a organismes eucariotes (ribosomes 60 S), i és produïda pel bacteri Streptomyces griseus. Té un ús estès en la investigació biomèdica per inhibir la síntesi de proteïnes en cèl·lules eucariotes in vitro.[3]
Referències
[modifica]- ↑ Gu Z, Harrod R, Rogers EJ, Lovett PS «Anti-peptidyl transferase leader peptides of attenuation-regulated chloramphenicol-resistance genes». Proc. Natl. Acad. Sci. U.S.A., 91, 12, juny 1994, pàg. 5612–6. PMC: 44046. PMID: 7515506.
- ↑ Protein synthesis inhibitors: macrolides mechanism of action animation. Classification of agents Arxivat 2008-12-26 a Wayback Machine. Pharmamotion. Author: Gary Kaiser. The Community College of Baltimore County. Retrieved on July 31, 2009
- ↑ Prescott, L.M.. Microbiología. McGraw-Hill Interamericana de España, S.A.U., 1999. ISBN 84-486-0261-7.
