Reacció de Heck
La reacció de Heck, també coneguda com a reacció de Mizoroki-Heck, és una reacció orgànica de formació d'alquens substituïts a través de la reacció catalitzada per compostos de pal·ladi d'un halur insaturat (aril o alquenil) amb un alquè en presència d'una base.[1][2]

Aquesta reacció va ser descoberta pel químic nord-americà R. F. Heck el 1970.
Història
[modifica]La reacció original de Tsutomu Mizoroki (1971) descriu l'acoblament entre iodobenzè i estirè en metanol per formar estilbè a 120 °C (autoclau) amb acetat de potassi com a base i clorur de pal·ladi com a catalitzador. Aquest treball va ser una extensió de treballs anteriors de Fujiwara (1967) sobre l'acoblament per mitjà de Pd(II) d'arens (Ar-H) i alquens[3][4] i treballs anteriors de Heck (1969) sobre l'acoblament d'halurs arilmercúrics (ArHgCl) amb alquens que utilitzen una quantitat estequiomètrica d'una espècie de pal·ladi(II).[5]
 |
| Mizoroki 1971 |
|---|
El 1972 Heck va reconèixer la publicació Mizoroki i va detallar els treballs descoberts independentment. Les condicions de reacció difereixen en el catalitzador utilitzat (acetat de pal·ladi) i la càrrega del catalitzador (0,01 eq.), la base utilitzada (una amina obstaculitzada) i l'absència de dissolvent.[6][7]
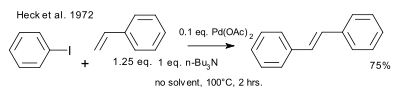 |
| Heck 1972 |
|---|
En aquestes reaccions, el catalitzador actiu Pd(0) (vegeu mecanisme de reacció) està format per la coordinació de Pd amb l’alquè.
El 1974 Heck va introduir lligands de fosfina a l'equació.[8]
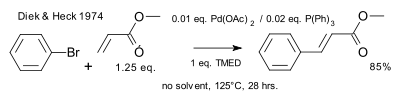 |
| Heck reaction 1974 phosphines |
|---|
Mecanisme
[modifica]El cicle catalític per a la reacció de Heck implica una sèrie de transformacions al voltant del catalitzador de pal·ladi.

Referències
[modifica]- ↑ Organic Chemistry Warren, Warren Clayren.
- ↑ Solomons, Jonh Wiley, 2a edició
- ↑ Moritani, Ichiro; Fujiwara, Yuzo «Aromatic substitution of styrene-palladium chloride complex». Tetrahedron Letters, 8, 12, 1-1967, pàg. 1119–1122. DOI: 10.1016/S0040-4039(00)90648-8.
- ↑ Fujiwara, Yuzo; Moritani, Ichiro; Danno, Sadao; Asano, Ryuzo; Teranishi, Shiichiro «Aromatic substitution of olefins. VI. Arylation of olefins with palladium(II) acetate». Journal of the American Chemical Society, 91, 25, 01-12-1969, pàg. 7166–7169. DOI: 10.1021/ja01053a047.
- ↑ Heck, Richard F. «Mechanism of arylation and carbomethoxylation of olefins with organopalladium compounds». Journal of the American Chemical Society, 91, 24, 11-1969, pàg. 6707–6714. DOI: 10.1021/ja01052a029.
- ↑ Heck, R. F.; Nolley, J. P. «Palladium-catalyzed vinylic hydrogen substitution reactions with aryl, benzyl, and styryl halides». The Journal of Organic Chemistry, 37, 14, 7-1972, pàg. 2320–2322. DOI: 10.1021/jo00979a024.
- ↑ Mizoroki, Tsutomu; Mori, Kunio; Ozaki, Atsumu «Arylation of Olefin with Aryl Iodide Catalyzed by Palladium». Bulletin of the Chemical Society of Japan, 44, 2, 2-1971, pàg. 581–581. DOI: 10.1246/bcsj.44.581.
- ↑ Dieck, H. A.; Heck, R. F. «Organophosphinepalladium complexes as catalysts for vinylic hydrogen substitution reactions». Journal of the American Chemical Society, 96, 4, 2-1974, pàg. 1133–1136. DOI: 10.1021/ja00811a029.
