Teràpia de reemplaçament enzimàtic
La teràpia de reemplaçament enzimàtic (ERT) és un tractament mèdic que consisteix en el reemplaçament d'un enzim en pacients en què l'enzim en particular és deficient o absent. Normalment això es subministra al pacient per mitjà d'una sonda intravenosa (IV) de perfusió amb l'enzim. La teràpia de reemplaçament enzimàtic només està disponible per a algunes malalties lisosomals: la malaltia de Gaucher, la malaltia de Fabry, MPS I, MPS VI i la malaltia d'emmagatzematge de glucogen tipus II. La teràpia de reemplaçament enzimàtic no "tracta" la malaltia de base, només els símptomes
La teràpia de reemplaçament enzimàtic és una tècnica mitjançant la qual es pretén proveir els lisosomes de la cèl·lula amb la quantitat apropiada d'enzims que li són deficitaris o absents per tal de poder processar el material no degradat que s'hi ha acumulat. Aquesta acumulació de material és molt tòxica per la cèl·lula, i això provoca malalties d'acumulació lisosomal (LSD).[1] N'hi ha unes 40 de diferents, depenent del tipus de material acumulat
Aquesta teràpia s'encarrega de tractar aquestes malalties des d'un punt de vista simptomàtic[2] cap al disseny d'un tractament per suplementar aquests enzims; malgrat tot, no és una cura definitiva sinó que intenta atenuar-ne la manifestació

Història
[modifica]El concepte de teràpia de reemplaçament enzimàtic per malalties d'acumulació lisosomal va ser postulat el 1964 per Christian de Duve. De Duve partia del punt que: “qualsevol substància que sigui adquirida intracel·lularment en un procés d'endocitosi és probable que acabi dins els lisosomes”.
En aquell moment la biologia no havia evolucionat suficientment per entendre la base de l'ERT i tampoc per poder utilitzar enzims lisosomals com a productes farmacèutics. La relació entre l'endocitosi i els lisosomes ja era ben coneguda, però el concepte LDS era nou en aquell moment i més encara les consegüents teràpies. Aquestes, com l'ERT, sols s'havien postulat teòricament però els faltava suport experimental, que va arribar a partir dels estudis fets sobre la malaltia de Pompe. Immediatament es va començar a aplicar el concepte d'ERT pel tractament dels pacients amb aquesta malaltia, però aquests intents no van tenir èxit
En un primer moment es van postular dos models d'ERT:
- La subministració d'enzims lisosomals amb senyal de reconeixement específica que permetia la correcta absorció, ja que als malalts els en mancava. Aquests enzims s'obtenien a partir del cultiu de cèl·lules de pacients amb mucopolisacaridosi (MPS)
- La subministració d'enzims lisosomals recombinats a partir de plasma de cèl·lules vives. Aquests enzims eren recombinats amb senyal de mannosa-6-fosfat (M6P), la qual els permetia entrar als lisosomes i solucionar-ne la manca.
El segon model és el que va agafar més força en el món científic i se'n va continuar la recerca. S'han requerit al voltant de quatre dècades per poder desenvolupar enzims comercials per l'ús farmacèutic com la glucocerebrosidasa (per la malaltia de Gaucher) o α-galactosidasa (per la malaltia de Fabry).
Tècnica d'obtenció d'enzims
[modifica]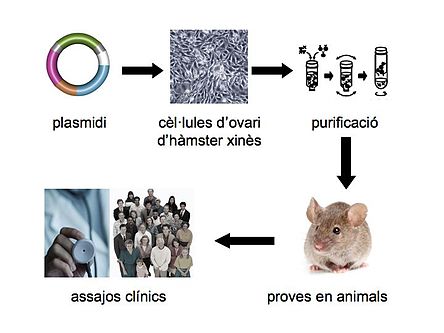
Per a la síntesi dels enzims que manquen en el lisosoma es recorre a l'ús de tècniques d'enginyeria genètica. Aquest fet implica la producció in vitro d'ADN recombinant a partir de la implantació del gen que codifica per l'enzim amb un vector (ADN animal, humà o bé un plasmidi d'una cèl·lula vegetal com s'ha dut a terme recentment). Després d'aquest primer pas, l'ADN recombinant té la capacitat de produir l'enzim funcional; no obstant cal treure'l de la cèl·lula i purificar-lo abans de convertir-lo en un medicament terapèutic per ser administrat als pacients. Posteriorment, els enzims són barrejats amb una solució que és apte per ser injectada al cos de forma intravenosa. Les cèl·lules capten els enzims, que es dirigeixen als lisosomes per dur a terme la catàlisi dels substrats que s'han anat acumulant
Les injeccions es realitzen un cop per setmana o cada quinze dies depenent de la malaltia, en dosis determinades pel pes corporal. Aquestes poden durar entre 20 i 30 minuts fins a unes hores després en funció de la teràpia que requereix la malaltia. Aquesta tècnica no és curativa, ja que el pacient haurà de seguir el tractament al llarg de la seva vida. Malgrat això, a partir dels resultats clínics que s'han observat es pot determinar que l'ERT permet millorar la supervivència, augmentar la qualitat de vida i la capacitat per dur a terme les activitats de la vida quotidiana, ja que suavitza els símptomes de la malaltia
Aplicacions
[modifica]La teràpia de reemplaçament enzimàtic és aplicable tan sols a algunes de les aproximadament quaranta malalties d'acumulació lisosòmica. Les malalties que poden ser tractades són:
- Malaltia de Gaucher[3]
- Malaltia de Fabry[4]
- Mucopolisacaridosis Tipus I (Gargolisme o Malaltia de Hurler)
Mentrestant, s'està investigant sobre el possible tractament de:
- Mucopolisacaridosis Tipus II (Síndrome de Hunter)
- Mucopolisacaridosis Tipus VI (Malaltia de Maroteaux-Lamy)
- Glucogenosis Tipus II (Malaltia de Pompe)[5]
- Malaltia de Niemann-Pick Tipus B
Limitacions
[modifica]Encara que l'ERT està ajudant a milers de persones a tenir una vida més saludable i dins la normalitat, hem de tenir en compte que té certes limitacions i que, per tant, la ciència està buscant noves vies d'investigació per millorar la salut d'aquests pacients.
Aquesta teràpia implica la introducció d'enzims eficaços perquè els lisosomes funcionin correctament, però el següent pas seria la teràpia gènica, en què el mateix cos produiria l'enzim i no dependria forçosament de la teràpia.
La limitació més gran a la qual s'enfronta aquesta teràpia és que, mentre que la majoria d'òrgans milloren davant el tractament perquè l'enzim treballa amb eficàcia, sembla que no redueix les acumulacions lisosomals en el sistema nerviós central. Això és perquè en el cervell hi ha una membrana protectora que el rodeja, anomenada barrera hematoencefàlica, que l'enzim administrat no pot travessar, de manera que no té cap efecte. Així doncs, les ERT es limiten a les malalties d'acumulació lisosomal que no afecten el cervell.
És una tècnica eficaç i generalment ben tolerada, però pot presentar efectes adversos, sovint relacionats amb anticossos (tot i que les reaccions anafilàctiques tenen una freqüència menor a un 1%).
A més a més, aquesta teràpia és més efectiva si s'inicia quan la malaltia està poc avançada, la qual cosa requereix una identificació precoç dels pacients, bastant complicat donat que no són malalties gaire freqüents.
Cal destacar, per acabar, que el cost de les ERT continua sent un limitant pels pacients sobretot dels països subdesenvolupats o en vies de desenvolupament.
Referències
[modifica]- ↑ «FEEL: Foro Español para Enfermedades Lisosomales». Arxivat de l'original el 2011-09-02. [Consulta: 15 novembre 2011].
- ↑ «P. Sanjurjo Crespo, L. Aldámiz-Echevarría, A. Baldellou Vázquez. Síntomas guía de las enfermedades lisosomales. Una orientación para el pediatra general.». Arxivat de l'original el 2011-09-05. [Consulta: 15 novembre 2011].
- ↑ [1]Gaucher Disease: “National Gaucher Fundation”
- ↑ [2]Fabry Disease: “ National Fabry Disease Fundation”
- ↑ «Pompe Disease: “National Institute of Neurological Disorders and Stroke”». Arxivat de l'original el 2011-11-22. [Consulta: 15 novembre 2011].
Bibliografia
[modifica]- Mehta A, Beck M, Sunder-Plassmann G, editors. Fabry Disease: Perspectives from 5 years of FSO. Oxford PharmaGenesis. 2006; ISBN 1-903539-03-X
- Beutler E. Enzyme Replacement in Gaucher Disease. PLoS Med. 2004 November; 1(2): e21. Published online 2004 November 30. PMCID: PMC529421. doi:10.1371/journal.pmed
- Bailey, L., (January 31, 2008) "An Overview of Enzyme Replacement Therapy for Lysosomal Storage Diseases" OJIN: The Online Journal of Issues in Nursing Vol. 13, No. 1, Manuscript 3
- Beck M. New therapeutic options for lysosomal storage disorders: enzyme replacement, small molecules and gene therapy. [Journal Article, Review]. Hum Genet 2007 Mar; 121(1):1-22
- Burrow TA, Hopkin RJ, Leslie ND, et al. Enzyme reconstitution/replacement therapy for lysosomal storage diseases. [Journal Article, Research Support, N.I.H., Extramural, Review] Curr Opin Pediatr 2007 Dec; 19(6):628-35
