Vaccí contra la COVID-19


El vaccí contra la COVID-19 o vacuna contra la COVID-19[1] és una vacuna destinada a proporcionar immunitat adquirida contra la COVID-19. Abans de la pandèmia COVID-19, els treballs per desenvolupar una vacuna contra les malalties del coronavirus SARS i MERS van establir un coneixement considerable sobre l'estructura i la funció dels coronavirus, que van accelerar el desenvolupament ràpid durant principis del 2020 de variades plataformes tecnològiques per a una vacuna contra la COVID-19.[2] El 10 de gener de 2020, les dades de la seqüència genètica del virus SARS-CoV-2 es van compartir a través de GISAID i, el 19 de març, la indústria farmacèutica mundial va anunciar un compromís important per abordar la COVID-19.[3]
En els assaigs de fase III, diverses vacunes COVID-19 van demostrar eficàcia fins al 95% en la prevenció d'infeccions simptomàtiques COVID-19.[4]
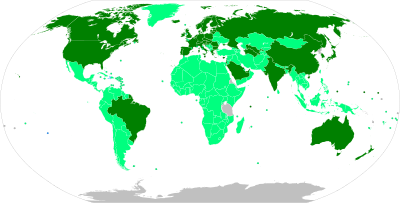
Les autoritats reguladores nacionals han aprovat 40 vacunes per a ús públic:[5]
- una vacuna d'ADN: ZyCoV-D[6]
- quatre vacunes d'ARN (vacuna de Pfizer-BioNTech,[7] vacuna de Moderna[8] Walvax, i Gemcovac
- dotze vacunes inactivades convencionals:[9] BBIBP-CorV, de l'Acadèmia Xinesa de Ciències Mèdiques, CoronaVac, Covaxin, CoviVac, COVIran Barekat, FakhraVac, Minhai, QazVac, WIBP-CorV, Turkovac i VLA2001.
- sis vacunes amb vectors vírics: Sputnik Light, Sputnik V, la vacuna d'Oxford-AstraZeneca, Convidecia, vacuna de Janssen i iNCOVACC.
- setze vacunes peptídiques o de subunitats:Abdala, CNBG, Corbevax, COVAX-19, EpiVacCorona, IndoVac, MVC-COV1901, Noora, Novavax, Razi Cov Pars, Sanofi–GSK, Soberana 02, Soberana Plus, V-01 i ZF2001
- una vacuna de partícules similivíriques: CoVLP
El juliol de 2021 hi havia 330 vacunes estaven en diverses etapes de desenvolupament, amb 102 fase preclínica, 30 en assaigs de fase I-II, 25 en fase III i 8 en fase IV.[5]
Molts països han implementat plans de distribució per fases que donen prioritat a aquells amb major risc de complicacions, com ara la gent gran, i aquells amb un alt risc d'exposició i transmissió, com els treballadors sanitaris.[10] Stanley Plotkin i Neal Halsey van escriure un article publicat al gener de 2021 per Clinical Infectious Diseases que instava a utilitzar una dosi única per estendre la vacunació a tantes persones com sigui possible fins que millorés la disponibilitat de la vacuna.[11] Diversos altres articles i mitjans van proporcionar proves per retardar les segones dosis en la mateixa línia de raonament.[12][13][14]
Al 17 de desembre de 2021, s'han administrat a tot el món 8,63 mil milions de dosis de vacuna COVID-19 segons els informes oficials de les agències nacionals de salut, el que significa que un 56.6% de la població mundial hauria rebut almenys una dosi, però que aquest percentatge baixa a un 7,6% en els països de renda baixa.[15] El desembre de 2020, els països havien encarregat més de 10.000 milions de dosis de vacuna,[16] amb aproximadament la meitat de les dosis adquirides pels països amb ingressos elevats que només representaven el 14% de la població mundial.[17]
Tipus de vacunes
[modifica]A gener del 2021 hi han nou plataformes tecnològiques diferents, amb la tecnologia de nombroses vacunes candidates sense definir, estaven en recerca i desenvolupament durant el 2020, per crear una vacuna eficaç contra la COVID-19.[5][18] La majoria de les plataformes de vacuna candidates en assaigs clínics a partir de setembre se centren en la proteïna S del coronavirus i les seves variants com a antigen primari de la COVID-19.[18] Les plataformes que es van desenvolupar el 2020 van incloure tecnologies d'àcids nucleics (ADN i ARN missatger amb nucleòsids modificats), vectors vírics que no es reprodueixen, pèptids, proteïnes recombinants, virus vius atenuats i virus inactivats.[2][18][19][20]
Moltes tecnologies de vacunes que s'estan desenvolupant per al COVID-19 no són com les vacunes que ja s'utilitzen per prevenir la grip, sinó que utilitzen estratègies de "nova generació" tenint en compte els mecanismes d'infecció per COVID-19.[2][18][20] Les plataformes vacunals en desenvolupament poden millorar la flexibilitat per a la manipulació de l'antigen i l'eficàcia dels contra els mecanismes concrets de la infecció per COVID-19 en subgrups de població susceptible, com ara treballadors sanitaris, gent gran, nens,[21] dones embarassades i persones amb els seus sistemes immunitaris debilitats.[18][20]
Vacunes d'ARN
[modifica]Una vacuna d'ARN conté ARN que, quan s'introdueix en un teixit, actua com a ARN missatger (ARNm) per fer que les cèl·lules construeixin la proteïna estranya i estimulin una resposta immunitària adaptativa que ensenya al cos a identificar i destruir el patogen o les cèl·lules canceroses corresponents. Les vacunes d'ARN sovint, però no sempre, utilitzen ARN missatger amb nucleòsids modificats. El lliurament d'ARNm s'aconsegueix mitjançant una coformulació de la molècula en nanopartícules de lípids que protegeixen les cadenes d'ARN i ajuden a la seva absorció a les cèl·lules.[22][23][24][25]
Les vacunes contra l'ARN van ser les primeres vacunes contra la COVID-19 autoritzades als Estats Units i a la Unió Europea.[26][27] A gener de 2021, les vacunes autoritzades d'aquest tipus són la vacuna de Pfizer-BioNTech
Les reaccions al·lèrgiques greus són rares.[30] El desembre de 2020, 1.893.360 primeres dosis d'administració de vacuna Pfizer–BioNTech van donar lloc a 175 casos de reacció al·lèrgica greu, dels quals 21 van ser anafilaxi.[31] Per a 4.041.396 administracions de dosi de vacuna de Moderna el desembre de 2020 i gener de 2021, només es van informar deu casos d'anafilaxi.[31] Les nanopartícules de lípids van ser probablement responsables de les reaccions al·lèrgiques.[31]
Vacunes amb adenovirus com a vectors
[modifica]Aquestes vacunes són exemples de vacunes de vectors vírics que no es reprodueixen, utilitzant una closca d'adenovirus que conté ADN que codifica una proteïna del SARS-CoV-2.[32][33] Els adenovirus d'aquestes vacunes no es reprodueixen, és a dir, que no formen partícules de virus noves, sinó que produeixen només l'antigen que provoca una resposta immune sistèmica.[32]
El gener de 2021, les vacunes autoritzades d'aquest tipus són la vacuna d'Oxford-AstraZeneca britànica,
La Convidecia i la vacuna de Janssen consten d'una sola injecció, així ofereixen una logística menys complicada; i es poden emmagatzemar sota refrigeració normal durant uns mesos.[34][35]
Sputnik V utilitza Ad26 per a la seva primera dosi, que és la mateixa que l'única dosi de Janssen, i Ad5 per a la segona dosi, que és la mateixa que l'única dosi que Convidecia.[36]
Vacunes de virus inactivats
[modifica]Les vacunes inactivades[37] consisteixen en partícules de virus que s'han cultivat i que després es maten mitjançant un mètode com la calor o el formaldehid per tal que perdin la capacitat de producció de malalties, però que mantenen l'aptitud d'estimular una resposta immunitària.[38]
A partir de gener de 2021, les vacunes autoritzades d'aquest tipus són la CoronaVac xinesa, BBIBP-CorV
Vacunes de subunitats
[modifica]Les vacunes de subunitats presenten un o més antígens sense introduir partícules de patògens sencers.[43] Els antígens implicats són sovint subunitats proteiques, però poden ser qualsevol molècula que sigui un fragment del patogen.[44]
A gener de 2021, l'única vacuna autoritzada d'aquest tipus era la vacuna peptídica russa EpiVacCorona.[45] Les vacunes en assaigs clínics inclouen la vacuna de Novavax i RBD-Dimer.[5] La vacuna V451 es trobava prèviament en assaigs clínics, que van interrompre perquè es va trobar que la vacuna pot causar resultats incorrectes per a les proves posteriors del VIH.
Altres tipus
[modifica]Altres tipus de vacunes que es troben en assaigs clínics inclouen múltiples vacunes d'ADN amb plasmidi,
S’estan desenvolupant i estudiant vacunes orals i intranasals.[28]
Els científics van investigar si les vacunes existents per a afeccions no relacionades podrien reforçar el sistema immunitari i disminuir la gravetat de la infecció per COVID-19.[56] Hi ha proves experimentals que demostren que la vacuna BCG contra la tuberculosi té efectes inespecífics sobre el sistema immunitari, però no hi ha proves que indiquin que aquesta vacuna sigui efectiva contra la COVID-19.[57][58]
Formulació
[modifica]Diverses vacunes utilitzen adjuvants per millorar la immunogenicitat.[18] Un adjuvant immunològic és una substància formulada amb una vacuna per elevar la resposta immunitària a un antigen, com el virus COVID-19 o el virus de la grip.[59][60] Els adjuvants utilitzats en la formulació de vacunes contra la COVID-19 poden ser particularment eficaços per a tecnologies que utilitzen el virus inactivat i vacunes recombinants basades en proteïnes o basades en vectors.[60] Les sals d'alumini, conegudes com a "alum", van ser el primer adjuvant utilitzat per a les vacunes autoritzades[61] i són l'adjuvant d'elecció en aproximadament el 80% de les vacunes adjuvantades.[60] L'adjuvant d'alum inicia diversos mecanismes moleculars i cel·lulars per millorar la immunogenicitat, inclosa l'alliberament de citocines proinflamatòries.[59][60]
Planificació i desenvolupament
[modifica]S'avaluen diversos passos al llarg de tota la ruta de desenvolupament, incloent-hi:[19][62]
- nivell de toxicitat acceptable de la vacuna (la seva seguretat),
- dirigit a poblacions vulnerables,
- necessitat d'avenços en l'eficàcia de la vacuna,
- la durada de la protecció de la vacunació,
- sistemes especials de lliurament (com ara oral o nasal, en lloc de la injecció),
- règim d'administració (primera dosi, segona dosi...),
- característiques d'estabilitat i emmagatzematge,
- autorització d'ús d'emergència abans de la llicència formal,
- fabricació òptima per poder subministrar milers de milions de dosis i
- difusió de la vacuna autoritzada.
Al 27 de març de 2021, s'havien administrat a tot el món 541,05 milions de dosis de vacuna contra la COVID-19 segons informes oficials d'agències nacionals de salut recopilades per Our World in Data.[63]
El 17 de febrer de 2021, a L'Estat espanyol s'havien administrat 2,69 milions de dosis de vacunes (5,75/100 habitants).[63]
Història
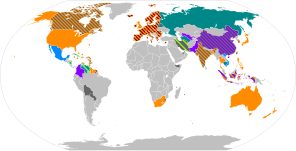
[modifica]Després d'aïllar el SARS-CoV-2 el desembre de 2019,[64] la seva seqüència genètica es va publicar l'11 de gener de 2020, provocant una resposta internacional urgent per preparar-se per a un brot i accelerar el desenvolupament d'una vacuna contra la COVID-19.[65][66][67] Des de principis del 2020, el desenvolupament de vacunes es va accelerar mitjançant una col·laboració sense precedents a la indústria farmacèutica multinacional i entre governs.[68] A juny de 2020, corporacions, governs, organitzacions sanitàries internacionals i grups de recerca universitaris van invertir desenes de milers de milions de dòlars per desenvolupar desenes de candidats a la vacuna i preparar-se per a programes globals de vacunació contra la infecció per COVID-19.[66][69][70][71] Segons la Coalició per a les Innovacions en Preparació per Epidèmies (CEPI), la distribució geogràfica del desenvolupament de vacunes COVID-19 fa que les entitats nord-americanes tinguin al voltant del 40% de l'activitat en comparació amb el 30% a Àsia i Austràlia, el 26% a Europa i alguns projectes a Amèrica del Sud i Àfrica.[65][68]
El febrer de 2020, l'Organització Mundial de la Salut (OMS) va dir que no esperava que una vacuna contra el SARS-CoV-2, el virus causant, estigués disponible en menys de 18 mesos.[72] La ràpida taxa d'infecció de COVID-19 a tot el món durant principis del 2020 va estimular les aliances internacionals i els esforços governamentals per organitzar amb urgència recursos per fabricar múltiples vacunes en terminis reduïts,[73] amb quatre candidats vacunats que van entrar a l'avaluació humana el març del 2020.[65][74]
El 24 de juny de 2020, la Xina va aprovar la vacuna de CanSino per a ús limitat a l'exèrcit i dues vacunes contra virus inactivats per a ús d'emergència en ocupacions d'alt risc.[75] L'11 d'agost de 2020, Rússia va anunciar l'aprovació de la seva vacuna Sputnik V per a ús d'emergència, tot i que un mes després només es van distribuir petites quantitats de la vacuna per al seu ús fora de l'assaig de fase III.[76]
El 20 de novembre de 2020, l'associació Pfizer–BioNTech va presentar una sol·licitud EUA a la Food and Drug Administration (FDA) per a la vacuna d'ARNm BNT162b2 (ingredient actiu tozinameran).[77][78] El 2 de desembre de 2020, l'Agència de Regulació de Medicaments i Productes Sanitaris (MHRA) del Regne Unit va aprovar temporalment la regulació de la vacuna de Pfizer-BioNTech,[79][80] convertint-se en el primer país que va aprovar aquesta vacuna i el primer país del món occidental per aprovar l'ús de qualsevol vacuna contra la COVID-19.[81][82][83] A partir del 21 de desembre, molts països i la Unió Europea[84] han autoritzat o aprovat la vacuna de Pfizer-BioNTech contra la COVID-19. Bahrain i els Emirats Àrabs Units van concedir una autorització d'emergència per a la comercialització de BBIBP-CorV, fabricat per Sinopharm.[85][86] L'11 de desembre de 2020, la FDA dels Estats Units va concedir una autorització d'ús d'emergència (EUA) per a la vacuna Pfizer-BioNTech contra la COVID-19.[87] Una setmana més tard, EUA va concedir una autorització per mRNA-1273, la vacuna de Moderna.[88][89][90]
La Gam-COVID-Vac (Sputnik V) russa creà en el seu moment un cert escepticisme tècnic relacionat amb els resultats de les proves inicials,[91][92] una vegada finalitzada la fase III d'un assaig clínic amb 20.000 participants havia demostrat ser segura i altament eficaç com a protecció contra el virus.[93]
El 31 de març de 2021, el govern rus va anunciar que havia registrat la primera vacuna COVID-19 per a animals.[94] Amb el nom de Carnivac-Cov, és una vacuna inactivada per a animals carnívors, incloses les mascotes, dirigida a prevenir les mutacions que es produeixen durant la transmissió interspècie del SARS-CoV-2.[95]
El juny de 2021, un informe va revelar que la vacuna UB-612, desenvolupada per la COVAXX nord-americana, era una empresa iniciada per obtenir beneficis pel fundador de Blackwater, Erik Prince. En una sèrie de missatges de text dirigits a Paul Behrends, l'últim col·laborador reclutat per al projecte COVAXX, Prince va descriure les possibilitats d'obtenir beneficis en vendre les vacunes COVID-19. COVAXX no va proporcionar dades dels assaigs clínics sobre seguretat o eficàcia. La responsabilitat de crear xarxes de distribució es va assignar a una entitat amb seu a Abu Dhabi, que es va esmentar com a "Windward Capital" al capçal de COVAXX, però que en realitat era Windward Holdings. L'únic accionista de la firma, que gestionava "activitats professionals, científiques i tècniques", era Erik Prince. El març de 2021, COVAXX va recaptar 1.350 milions de dòlars en una ubicació privada.[96]Vacunes desenvolupades a Catalunya
[modifica]Hi ha diverses vacunes en desenvolupament a Catalunya, entre elles una de l'empresa farmacèutica multinacional Laboratoris Hipra d'Amer basada en proteïnes recombinants i una altra en col·laboració amb l'Hospital Clínic de Barcelona basada en ARN missatger.[97][98] També hi ha un assaig de la vacuna RUTI de l'Hospital Germans Trias i Pujol per comprovar si aquesta vacuna contra la tuberculosi és efectiva també contra la Covid, gràcies al fenomen de la immunitat entrenada monocitària.[99]
El 30 de març de 2023 la primera d'elles, amb el nom de Bimervax, va rebre finalment l'aval de l'Agència Europea del Medicament, que ja es va poder administrar com a recordatori a persones de més de 16 anys que haguessin rebut anteriorment una vacuna d'ARNm.
Assajos i autoritzacions de vacunes
[modifica]Els assaigs de fase I proven principalment la seguretat i la dosificació preliminar en algunes dotzenes de subjectes sans, mentre que els assaigs de fase II, després de l'èxit en la fase I, avaluen la immunogenicitat, els nivells de dosi (eficàcia basats en biomarcadors) i els efectes adversos de la vacuna candidata, normalment en centenars de persones.[100][101] Un assaig de fase I-II consisteix en proves preliminars de seguretat i immunogenicitat, generalment aleatoritzat, controlat amb placebo, alhora que es determinen dosis més precises i efectives.[101] Els assajos de fase III solen implicar més participants en diversos llocs, inclouen un grup de control i proven l'eficàcia de la vacuna per prevenir la malaltia (un assaig "intervencionista" o "pivotal"), mentre es monitoritza els efectes adversos en la dosi òptima.[100][101] La definició de seguretat, eficàcia i criteris clínics de la vacuna en un assaig de fase III pot variar entre els assaigs de diferents empreses, com ara definir el grau d'efectes secundaris, la infecció o la quantitat de transmissió, i si la vacuna prevé una COVID-19 moderada o severa.[102][103][104]
El disseny d'un assaig clínic en curs es pot modificar com a "disseny adaptatiu" si l'acumulació de dades de l'assaig proporciona informació inicial sobre una eficàcia positiva o negativa del tractament.[105][106] Els dissenys adaptatius dels assaigs clínics en fase II-III en curs amb vacunes candidates poden escurçar la durada dels assaigs i utilitzar menys subjectes, possiblement accelerant les decisions per a la finalització primerenca o l'èxit, evitant la duplicació dels esforços de recerca i millorant la coordinació dels canvis de disseny de l'assaig Solidaritat a tot el món.[105][107]
Vacunes aprovades
[modifica]Les autoritats reguladores nacionals han concedit autoritzacions d'ús d'emergència per a deu vacunes. Tres d'aquestes han estat aprovades per a ús d'emergència o ús complet per les autoritats reguladores estrictes (SRA) reconegudes per l'OMS.
Llistat de vacunes autoritzades
[modifica]| Nom comú | Tipus (tecnologia) | País d'origen | Primera autorització | Notes |
|---|---|---|---|---|
| Autoritzades a més de 10 països | ||||
| Oxford–AstraZeneca | Vector d'adenovirus | Regne Unit, Suècia | Desembre 2020 | |
| Pfizer–BioNTech | ARN | Alemanya, Estats Units | Desembre 2020 | Tant les versions originals com les variants Òmicron. |
| Janssen (Johnson & Johnson) | Vector d'adenovirus | Estats Units, Països Baixos | Febrer 2021 | |
| Moderna
ARN |
Estats Units | Desembre 2020 | Tant les versions originals com les variants Òmicron | |
| Sinopharm BIBP | Inactivada | Xina | Juliol 2020 | |
| Sputnik V | Vector d'adenovirus | Rússia | Agost 2020 | |
| CoronaVac | Inactivada | Xina | Agost 2020 | |
| Novavax | Subunitats | Estats Units | Desembre 2021 | Una "vacuna de nanopartícules recombinants"[108] |
| Covaxin | Inactivada | Índia | Gener 2021 | |
| Valneva | Inactivada | França, Àustria | Abril 2022 | |
| Sanofi–GSK | Subunitats | França, Regne Unit | Novembre 2022 | Basat en Variant Beta |
| Sputnik Light | Vector d'adenovirus | Rússia | Maig 2021 | |
| Autoritzades entre 2 i 10 països | ||||
| Convidecia | Vector d'adenovirus | Xina | Juny 2020 | |
| Sinopharm WIBP | Inactivada | Xina | Febrer 2021 | |
| Abdala | Subunitats | Cuba | Juliol 2021 | |
| EpiVacCorona |
Subunitats | Rússia | Octubre 2020 | |
| Zifivax | Subunitats | Xina | Març 2021 | |
| Soberana 02 | Subunitats | Cuba, Iran | Juny 2021 | |
| CoviVac | Inactivada | Rússia | Febrer 2021 | |
| Medigen | Subunitats | Taiwan | Juliol 2021 | |
| QazCovid-in | Inactivada | Kazakhstan | Abril 2021 | |
| Minhai | Inactivada | Xina | Maig 2021 | |
| COVIran Barekat | Inactivada | Iran | Juny 2021 | |
| Soberana Plus | Subunitats | Cuba | Agost 2021 | |
| Corbevax |
Subunitats | Índia, Estats Units | Desembre 2021 | |
| Autoritzades en 1 país | ||||
| Acadèmia Xinesa de Ciències Mèdiques | Inactivada | Xina | Juny 2021 | |
| ZyCoV-D |
ADN | Índia | Agost 2021 | |
| FakhraVac | Inactivada | Iran | Setembre 2021 | |
| COVAX-19 | Subunitats | Austràlia, Iran | Octubre 2021 | |
| Razi Cov Pars | Subunitats | Iran | Octubre 2021 | |
| Turkovac | Inactivada | Turquia | Desembre 2021 | |
| Sinopharm CNBG | Subunitats | Xina | Desembre 2021 | Basat en variants originals, Beta i Kappa |
| CoVLP | Recombinant, Partícula similivírica | Canadà, Regne Unit | Febrer 2022 | |
| Noora | Subunitats | Iran | Març 2022 | |
| Skycovione | Subunitats | Corea del Sud | Juny 2022 | |
| Walvax | ARN | Xina | Setembre 2022 | |
| iNCOVACC | Vector d'adenovirus | Índia | Setembre 2022 | Vacuna nasal |
| V-01 | Subunitats | Xina | Setembre 2022 | |
| Gemcovac | ARN | Índia | Octubre 2022 | Vacuna d'ARN autoamplificant |
| IndoVac | Subunitats | Indonèsia | Octubre 2022 | |
Vacunes candidates
[modifica](Actualitzades fins a novembre de 2022)
Amb fase I acabada:
| Vacunes candidates Desenvolupadors, patrocinadors |
País d'origen | Tipus (tecnologia) |
Fase actual (participants) Disseny |
Fase finalitzada[a] (participants) Resposta immunitària |
Pendent autorització |
|---|---|---|---|---|---|
| Vacuna de Sanofi-GSK (VAT00002) Sanofi Pasteur, GSK |
França, Regne Unit | De subunitats | Fase III (37.430) Un grup paral·lel, multi-etapa, doble cec modificat, multi-armat, per avaluar l'eficàcia, la seguretat i la immunogenicitat de dues vacunes de proteïnes recombinants adjuvantades de SARS-CoV-2 (monovalents i bivalents). -19 en adults majors de 18 anys. Mai 2021 – Gen 2023, Kenya,[113] Mèxic,[114] Estats Units |
Fase I–II (1.160) Fase I-IIa (440): Immunogenicitat i seguretat de les formulacions de vacunes (amb o sense adjuvant) en adults sans de 18 anys o més.[115] Fase IIb (720): Immunogenicitat i seguretat de la vacuna amb adjuvant AS03 en adults de 18 anys o més.[116] Set 2020 – Set 2022, Estats Units |
Emergència (3+27=31)
|
| Nanocovax[121] Nanogen Pharmaceutical Biotechnology JSC |
Vietnam | Recombinant de la proteïna S (amb alumini com a adjuvant)[122][123] | Fase III (13.000) Adaptatiu, multicèntric, aleatoritzat, doble cec, controlat amb placebo Jun 2021–Jul 2022, Vietnam |
Fase I (620) Fase (60): marca oberta, escalat de la dosi. Fase II (560): aleatorització, doble cec, multicèntric, controlat amb placebo. Des 2020 – Jun 2021, Vietnam |
|
| UB-612 United Biomedical,Inc, COVAXX, DASA |
Brasil, Estats Units | De subunitats | Fase III (18.320) Fase IIb/III (7.320): aleatoritzat, multicèntric, doble cec, controlat amb placebo, resposta a la dosi. Fase III (11.000) Gen 2021 – Mar 2023, Taiwan (fase 2b/3), Índia (fase 3)[130] |
Fase I–II (3.910) Phase 1 (60): Estudi obert Phase IIa (3.850): Estudi controlat amb placebo, aleatoritzat i cec a l'observador. Set 2020 – Gen 2021, Taiwan |
|
| SCB-2019 Clover Biopharmaceuticals,[135][136] Dynavax Technologies,[137] CEPI |
Xina | De subunitats de la proteïna S amb CpG 1018 combinat i coadjuvant d'alumini | Fase III (30.000) Fase II/III (30.000): Aleatori, doble cec, controlat Fase III (300): Doble cec, aleatoritzat, controlat. Mar 2021 – Oct 2022, Bèlgica, Brasil, Colòmbia, República Dominicana, Alemanya, Nepal, Panamà, Filipines, Polònia, Sud-àfrica, Ucraïna |
Fase I–II (950) Fase I (150): aleatoritzada, doble cec, controlada amb placebo, primera en humans. Fase II (800): multicèntric, doble cec, aleatoritzat, controlat.[138] Jun 2020 – Oct 2021, Austràlia (fase 1), Xina (fase 2) |
|
| S-268019 Shionogi |
Japó | De subunitats | Fase III (54.915) Fase II/III: Etiqueta oberta. Fase III: Aleatoritzat, cec per a l'observador i controlat per placebo. Oct 2021 – Dec Des, Japó (3,100), Vietnam |
Fase I–II (300) Aleatori, doble cec, controlat amb placebo, grup paral·lel. Des 2020 – Ago 2021, Japó |
|
| Vacuna de l'Hospital de la Xina Occidental Centres de Control i Prevenció de Malalties de la província de Jiangsu, Hospital de la Xina Occidental |
Xina | De subunitats (recombinant amb cèl·lules Sf9) | Fase III (40.000) Multicèntric, aleatoritzat, doble cec, controlat amb placebo. Jun 2021 – Feb 2022, Indonèsia, Kenya, Filipines |
Fase I–II (5.005) Phase I (45): Monocentre, aleatoritzat, controlat amb placebo, doble cec. Phase IIa (960): Centrocentre, aleatoritzat, doble cec, controlat amb placebo. Phase IIb (4.000): Centrocentre, aleatoritzat, doble cec, controlat amb placebo. Ago 2020 – Mai 2021, Xina |
|
| DelNS1-2019-nCoV-RBD-OPT Beijing Wantai Biological Pharmacy, Universitat de Hong Kong |
Xina, Hong Kong | Vector víric | Fase III (40.000) Multicèntric, aleatoritzat, doble cec, controlat amb placebo. Oct 2021 – Abr 2022, Filipines |
Fase I–II (895) Fase I (60+115=175) Fase II (720) Set 2020 – Set 2022, Xina (60), Hong Kong (115) |
|
| Versamune-CoV-2FC Farmacore Biotechnology, PDS Biotechnology Corporation, Facultat de Medicina de Ribeirão Preto |
Brasil, Estats Units | De subunitats | Fase III (30.000) Doble cec, controlat aleatoritzat. Ago–Des 2021, Brasil |
Fase I–II (360) Doble cec, controlat aleatoritzat. Mar–Ago 2021, Brasil |
|
| Vacuna de Walvax Acadèmia de Ciències Militars de l'Exèrcit Popular d'Alliberament, Walvax Biotech[153] |
Xina | ARN | Fase III (28.000) Multicèntric, aleatoritzat, doble cec, controlat amb placebo Mai – Oct 2021, Xina[154] |
Fase I–II (588) Fase I (168) Fase II (420) Jun 2020 – Mar 2022, Xina[155] |
|
| V-01 Livzon Mabpharm, Inc. |
Xina | De subunitats | Fase III (22.500) Global, multicèntric, aleatoritzat, doble cec, controlat amb placebo. Ago 2021–Mar 2023, Filipines |
Fase I (1.060) Fase I (180): Monocèntric, aleatoritzat, doble cec i controlat amb placebo. Fase II (880): Aleatori, doble cec i controlat amb placebo. Feb–Mai 2021, Xina |
|
| ARCT-154 (VBC-COV19-154 a Vietnam)[159][160][161] Arcturus Therapeutics, Vinbiocare |
Estats Units, Vietnam | ARN | Fase III (20.600) Fase IIIa (600): aleatoritzada, doble cec, controlada amb placebo. Fase IIIb (20.000): aleatoritzat, doble cec, controlat amb placebo.[162][163] Oct-Des 2021, Vietnam |
Fase I–II (400) Fase I (100): aleatoritzada, doble cec, controlada amb placebo. Fase II (300): aleatoritzat, doble cec, controlat amb placebo. Ago-Oct 2021, Vietnam[164] |
|
| ReCOV Jiangsu Rec-Biotechnology Co Ltd |
Xina | De subunitats (recombinant de dos components: espícula i proteïna RBD (cèl·lula CHO)) | Fase II–III (20.301) Multicèntric, aleatoritzat, doble cec, controlat amb placebo. Des 2021–Des 2022, Xina, Nova Zelanda |
Fase I (160) Primer en humans, aleatoritzat, doble cec, controlat amb placebo, de cerca de dosis. Jun–Des 2021, Nova Zelanda |
|
| BriLife (IIBR-100) L'Institut d'Investigació Biològica d’Israel |
Israel | Estomatitis vesicular com a vector (Recombinant) | Fase III (20.000) Aleatoritzat, multicèntric, controlat amb placebo. Set – Des 2021, Israel |
Fase I–II (1.040) Aleatoritzat, multicèntric, controlat amb placebo, escalat de dosis. Oct 2020 – Mai 2021, Israel |
|
| Vacuna de Zhongyianke Biotech–Liaoning Maokangyuan Biotech Zhongyianke Biotech, Liaoning Maokangyuan Biotech, Academy of Military Medical Sciences |
Xina | De subunitats (Recombinant) | Fase III (14.600) Multicentre internacional, aleatoritzat, doble cec, controlat amb placebo. Set 2021–?, Xina |
Fase I–II (696) Fase I (216): Aleatoritzada, controlada amb placebo, doble cec. Fase II (480): Monocentre, aleatoritzada, doble cec, controlada amb placebo.[172] Oct 2020 – Jul 2021, Xina |
|
| GX-19 (GX-19N) Genexine consortium,[176][177] International Vaccine Institute |
Corea del Sud | Vacuna d'ADN | Fase II–III (14.000) Aleatoritzat, doble cec, controlat amb placebo. Oct 2021 – Oct 2022, Indonèsia, Seül |
Fase I–II (410) Fase I-II (170+210+30): Multicèntric, alguns de marca oberta, altres de doble cec, de braç únic, aleatoritzats i controlats amb placebo Jun 2020 – Jul 2021, Seül |
|
| GRAd-COV2 ReiThera, Institut Nacional de Malalties Infeccioses "Lazzaro Spallanzani" |
Itàlia | Vector d'adenovirus (virus de ximpanzé modificat, GRAd) | Fase III (10.300) Aleatoritzat, estratificat, observador-cec, controlat amb placebo. Mar – Mai 2021, Itàlia |
Fase I (90) Els subjectes (dos grups: 18-55 i 65-85 anys) que rebien aleatòriament una de les tres dosis creixents de GRAd-COV2 o un placebo, que després es controlaven durant un període de 24 setmanes. El 93% dels subjectes que van rebre GRAd-COV2 van desenvolupar anticossos. Ago – Des 2020, Roma |
|
| Inovio COVID-19 Inovio, CEPI, Institut Nacional de Salut de Corea, Institut Internacional de Vacunes |
Corea del Sud, Estats Units | Plàsmid d'ADN lliurat per electroporació | Fase III (7.517) Aleatoritzada, controlada amb placebo, multicèntrica.[184] Nov 2020 – Gen 2023, Brasil, Colòmbia, Mèxic, Filipines, Estats Units |
Fase I–II (920) Fase Ia (120): Assaig obert. Fase Ib-IIa (160): assaig de dosis.[185] Fase II (640): aleatoritzat, doble cec, controlat amb placebo, cerca de dosis.[186] Abril 2020 – Feb 2022, Xina (fase II), Corea del Sud (fase Ib-IIa), Estats Units |
|
| DS-5670[187] Daiichi Sankyo[188] |
Japó | ARN | Fase II–III (5.028) Aleatori, comparador actiu, observador cec. Des 2021 – Jul 2023, Japó |
Fase I–II (152) Un estudi de fase 1/2 per avaluar la seguretat, la immunogenicitat i la dosi recomanada de DS-5670a en adults i ancians sans japonesos. Mar 2021 – Jul 2022, Japó |
|
| GBP510 SK Bioscience Co. Ltd., GSK |
Corea del Sud | De subunitats (Nanopartícula de proteïna recombinant amb coadjuvant amb AS03) | Fase III (4.000) Aleatoritzat, controlat activament, cec-observador, grup paral·lel, multicèntric.[192] Ago-Mar 2022, Corea del Sud |
Fase I–II (580) Fase I-II (260-320): controlat amb placebo, aleatoritzat, cec a l’observador i localitzador de dosis. Gen–Ago 2021, Corea del Sud |
|
| HGC019 Gennova Biopharmaceuticals, HDT Biotech Corporation[196] |
Índia, Estats Units | ARN | Fase II–III (4.400) Un estudi prospectiu, multicèntric, aleatoritzat, controlat activament (amb COVISHIELD), observador cec per avaluar la seguretat, la tolerabilitat i la immunogenicitat en adults sans. Fase II (400) Fase III (4.000) Set 2021 – ?, India |
Fase I–II (620) Estudi multi-centre aleatoritzat, de fase I/II, controlat amb placebo, de dosis, grup paral·lel, creuat, per avaluar la seguretat, la tolerabilitat i la immunogenicitat en subjectes adults sans. Estudi obert de fase I (120) en joves sans de 18 a 70 anys. Estudi de fase II (500) observador cec en joves sans de 18 a 75 anys. Abr 2021 – Oct 2021, Índia |
|
| KD-414 KM Biologics Co |
Japó | Inactivada | Fase II–III (2.000) Multicèntric, obert, no aleatoritzat. Oct 2021 – Mar 2023, Japó |
Fase I–II (210) Aleatori, doble cec, control amb placebo, grup paral·lel.[203] Mar 2021 – Des 2022, Japó |
|
| LYB001 Patronus Biotech |
Xina | Fase II–III (1,900) Fase II: aleatoritzada, doble cec, controlada amb placebo Fase III: amb un sol braç, de marca oberta expandida. Oct 2021 – ?, Laos |
Fase I (100) Aleatoritzat, doble cec, controlat amb placebo. Des 2021 – Feb 2022, Laos |
||
| AKS-452 Akston Biosciences, Centre Mèdic Universitari de Groningen |
Països Baixos | De subunitats | Fase II–III (1.600) Aleatori, doble cec, controlat amb placebo, grup paral·lel, multicèntric, adaptatiu, pont sense fissures. Oct 2021–Des 2022, Índia |
Fase I–II (112) No aleatoritzat, únic centre, d'etiqueta oberta, combinatòria. Abr–Set 2021, Països Baixos |
|
| AG0302-COVID‑19 AnGes Inc.,[209] AMED |
Japó | Plàsmid d'ADN | Fase II–III (500) Aleatoritzat, doble cec, controlat amb placebo[210] Lloc(s): Japó Durada: Nov 2020 – Mai 2021 |
Fase I–II (30) No aleatoritzat, monocentre, dues dosis Lloc(s): Osaka Durada: Jun 2020 – Nov 2020 |
|
| 202-CoV Shanghai Zerun Biotechnology Co., Ltd., Walvax Biotech |
Xina | Recombinant de la proteïna S (amb alumini com a adjuvant) | Fase II (1.056) Aleatoritzat, doble cec, controlat amb placebo. Jul–Des 2021, Xina |
Fase I (144) Aleatoritzat, doble cec, controlat amb placebo. Jul–Des 2021, Xina |
|
| Vacuna de Vaxart contra la COVID-19 Vaxart |
Estats Units | Vector víric | Fase II (896) Doble cec, multicèntric, aleatoritzat, controlat amb placebo, de dosi. Oct 2021 – Mar 2022, Estats Units |
Fase I (83) Fase Ia (35): doble cec, aleatoritzat, controlat amb placebo, primer en humans. Fase Ib (48): multicèntric, aleatoritzat, doble cec, controlat amb placebo. Sep 2020 – Ago 2021, Estats Units |
|
| PTX-COVID19-B[216] Providence Therapeutics |
Canadà | ARN | Fase II (890) Aleatori, dos braços, observador cec. Ago 2021–Feb 2022, Canadà |
Fase I (60) Primer en humà, cec per l'observador, aleatoritzat, controlat amb placebo.[218] Gen–Mai 2021, Canadà |
|
| Sense nom Ningbo Rong’an Biological Pharmaceutical Co., Ltd. |
Xina | Inactivada | Fase II (600) Aleatoritzat, doble cec, controlat amb placebo. Oct 2021 – Mar 2022, Xina |
Fase I (150) Aleatoritzat, doble cec, controlat amb placebo. Ago – Oct 2021, Xina |
|
| Sense nom Tsinghua University, Tianjin Medical University,[221] Walvax Biotech |
Xina | Vector víric | Fase II (360) Jul–Nov 2021, Xina |
Fase I (60) Mai–Jun 2021, Xina |
|
| INNA-051 Ena Respiratory |
Austràlia | Vector víric | Fase II (423) Aleatori, doble cec, controlat amb placebo. Mar – Des 2022, Austràlia |
Fase I (124) Aleatori, doble cec, controlat amb placebo. Jun – Oct 2021, Austràlia |
|
| mRNA-1283 Moderna |
Estats Units | ARN | Fase II (420) Aleatoritzat, estratificat, cec a l'observador. Des 2021 – Gen 2023, Estats Units |
Fase I (106) Estudi aleatoritzat, cec per a l'observador i amb dosis. Mar 2021 – Abr 2022, Estats Units |
|
| Sense nom
Ihsan Gursel, Consell d'Investigacions Científiques i Tecnològiques de Turquia |
Turquia | Partícula similivírica | Fase II (330) Assignació aleatòria, dosi paral·lela, doble cec, multi-centre. Jun – Set 2021, Turquia |
Fase I (36) doble cec, aleatoritzat, controlat amb placebo. Mar 2021 – Mar 2022, Turquia | |
| COH04S1 City of Hope Medical Center |
Estats Units | Vector víric | Fase II (240) Multicèntric, cec a l'observador, controlat per la vacuna a EUA, aleatoritzat. Ago 2021 – Jun 2023, Califòrnia |
Fase I (129) Estudi d’escalada de la dosi. Des 2020 – Nov 2022, Califòrnia |
|
| ABNCoV2 Bavarian Nordic.[232] Radboud University Nijmegen |
Dinamarca, Països Baixos | Partícula similivírica | Fase II (210) Assaig de dosi en un únic centre, seqüencial, amb etiqueta oberta. Ago-Des 2021, Alemanya |
Fase I (42) Assaig de dosi en un únic centre, seqüencial, amb etiqueta oberta. Mar–Des 2021, Països Baixos |
|
| A més de la catalana d'Hipra, podeu trobar la resta dels estudis en fase preclínica aquí en anglès | |||||
| PHH-1V Hipra[236] |
Espanya | De subunitats | Fase I–II (286) Fase I/IIa (30): aleatoritzat, controlat, cec per l'observador, escalada de dosi. Fase IIb (256): aleatoritzat, controlat, cec a l'observador. Ago–Des 2021, Espanya (fase I/IIa), Vietnam (fase IIb) |
Preclínic |
|
| Vacuna de CureVac (CVnCoV) CureVac, CEPI |
Alemanya | ARNm amb ARNmod[239] | Finalitzat (44.433) Fase2b/3 (39.693): Assaig multicèntric d'eficàcia i seguretat en adults. Fase3 (2.360+180+1.200+1.000=4.740): Aleatoritzat, cegat per l'observador, controlat amb placebo. Nov 2020 – Sep 2021, Argentina, Bèlgica, Colòmbia, República Dominicana, França, Alemanya, Mèxic, Països Baixos, Panamà, Perú, Espanya[244] |
Fase I–II (944) Phase 1 (284): Parcialment cec, controlat, amb dosi escalada per avaluar la seguretat, la reactogenicitat i la immunogenicitat. Fase 2a (660): Observador parcialment cec, multicèntric, controlat, amb confirmació de dosi. |
Emergència (1+27)=28
|
Vacunació heteròlega de sensibilització-reforç
[modifica]Alguns experts creuen que les pautes de vacunació heteròlega (vacunes diferents) per a la vacuna inicial de sensibilització i per la segona vacuna de reforç) poden augmentar la immunitat, i diversos estudis han començat a examinar aquest efecte.[248] Malgrat l'absència de dades clíniques sobre l'eficàcia i seguretat d'aquestes combinacions heteròlegues, el Canadà i diversos països europeus han recomanat una segona dosi heteròloga per a les persones que han rebut la primera dosi de la vacuna Oxford-AstraZeneca.[249]
| Primera dosi | Segona dosi | Dies entre dosis | Fase actual (participants), períodes i ubicacions |
|---|---|---|---|
| Oxford–AstraZeneca Pfizer–BioNTech |
Oxford–AstraZeneca Pfizer–BioNTech |
28 84 |
Fase II (820) Feb – Ago 2021, Regne Unit |
| Sputnik Light | Oxford–AstraZeneca Moderna BBIBP-CorV |
Fase II (121) Feb – Ago 2021, Argentina | |
| Oxford–AstraZeneca Pfizer–BioNTech |
Oxford–AstraZeneca Pfizer–BioNTech Moderna Novavax |
56 – 84 | Fase II (1.050) Mar 2021 – Set 2022, Regne Unit |
| Convidecia | ZF2001 | 28 56 |
Fase IV (120) Abr – Des 2021, Xina |
| Oxford–AstraZeneca | Pfizer–BioNTech | 28 | Fase II (676) Abr 2021 – Abr 2022, Espanya |
| Oxford–AstraZeneca Pfizer–BioNTech Moderna |
Pfizer–BioNTech Moderna |
28 112 |
Fase II (1.200) Mai 2021 – Mar 2023, Canadà |
| Pfizer–BioNTech Moderna |
Pfizer–BioNTech Moderna |
42 | Fase II (400) Mai 2021 – Gen 2022, França |
| Oxford–AstraZeneca | Pfizer–BioNTech | 28 21 – 49 |
Fase II (3.000) Mai – Des 2021, Àustria |
| Janssen | Pfizer–BioNTech Janssen Moderna |
84 | Fase II (432) Jun 2021 – Set 2022, Països Baixos |
Eficàcia
[modifica]L'eficàcia d'una nova vacuna es defineix per la seva eficàcia durant els assaigs clínics. L'eficàcia és el risc de contraure la malaltia per part dels participants vacunats de l'assaig en comparació amb el risc de contraure la malaltia per part dels participants no vacunats. Una eficàcia del 0% significa que la vacuna no funciona (idèntica al placebo). Una eficàcia del 50% significa que hi ha la meitat de casos d'infecció que en individus no vacunats.
No és senzill comparar l'eficàcia de les diferents vacunes perquè els assaigs es van realitzar amb diferents poblacions, geografies i variants del virus.[259][260] En el cas de COVID-19, una eficàcia de la vacuna del 67% pot ser suficient per frenar la pandèmia, però això suposa que la vacuna confereix immunitat esterilitzant, que és necessària per evitar la transmissió. L'eficàcia de les vacunes reflecteix la prevenció de la malaltia, un indicador deficient de transmissibilitat del SARS-CoV-2, ja que les persones asimptomàtiques poden ser altament infeccioses.[261] L'Administració d'Aliments i Fàrmacs (FDA) i l'Agència Europea de Medicaments (EMA) van establir un límit del 50% com a eficàcia necessària per aprovar una vacuna contra la COVID-19.[262][263] Amb l'objectiu d'una taxa de cobertura de vacunació de la població realista del 75% i, en funció del nombre reproductiu bàsic actual, s'espera que l'eficàcia necessària d'una vacuna contra la COVID-19 sigui d'un 70% com a mínim per prevenir una epidèmia i d'un 80% com a mínim per extingir-la. sense més mesures, com ara el distanciament social.[264]
En els càlculs d'eficàcia, la COVID-19 simptomàtica es defineix generalment com amb una prova de la PCR positiva i com a mínim un o dos d'una llista definida de símptomes de la COVID-19, tot i que les especificacions exactes varien entre assaigs. La ubicació de l'assaig també afecta l'eficàcia reportada perquè diferents països tenen prevalences diferents de variants del SARS-CoV-2. Els rangs següents són intervals de confiança del 95% tret que s'indiqui el contrari, i tots els valors són per a tots els participants independentment de l'edat. L'eficàcia contra la COVID-19 greu és la més important, ja que les hospitalitzacions i les defuncions són una càrrega de salut pública la prevenció de les quals és prioritària.[265] Les vacunes autoritzades i aprovades han mostrat les següents eficàcies:
| Vacuna | Eficàcia per gravetat de la COVID-19 | Localització de prova | Referències | ||
|---|---|---|---|---|---|
| Lleu o moderada[A] | Greu sense hospitalització ni mort[B] | Greu amb hospitalització o mort[C] | |||
| Oxford-AstraZeneca | 81% (60–91%)[D] | 100% (97.5% IC, 72–100%) | 100%[E] | Multinacional | [266] |
| 74% (68–82%)[F] | 100%[E] | 100%[E] | Estats Units | [267] | |
| Pfizer-BioNTech | 95% (90–98%)[G] | 66% (−125–96%)[H][G] | Multinacional | [269] | |
| 95% (90–98%)[G] | No notificat | No notificat | Estats Units | [268] | |
| Janssen | 66% (55–75%)[I][J] | 85% (54–97%)[J] | 100%[E][J][K] | Multinacional | [270] |
| 72% (58–82%)[I][J] | 86% (−9–100%)[J] | 100%[E][J][K] | Estats Units | ||
| 68% (49–81%)[I][J] | 88% (8–100%)[J] | 100%[E][J][K] | Brasil | ||
| 64% (41–79%)[I][J] | 82% (46–95%)[J] | 100%[E][J][K] | Sud-àfrica | ||
| Moderna | 94% (89–97%)[L] | 100%[E][M] | 100%[E][M] | Estats Units | [272] |
| BBIBP-CorV | 78% (65–86%) | 100%[E] | 100%[E] | Multinational | [273] |
| 79% (66–88%) | No notificat | 79% (26–94%)[H] | Multinational | [274] | |
| Sputnik V | 92% (86–95%) | 100% (94–100%) | 100%[E] | Rússia | [275] |
| CoronaVac | 51% (36–62%)[N] | 84% (58–94%)[N] | 100% (56–100%)[N] | Brasil | [276][277][278] |
| 84% (65–92%) | 100%[E] | 100% (20–100%)[H] | Turquia | [278] | |
| Covaxin | 78% (61–88%)[N] | 93% (57–100%)[N] | Índia | [279][font poc fiable?] | |
| Sputnik Light | 79%[E] | No notificat | No notificat | Rússia | [280] |
| Convidecia | 66%[E][N] | 91%[E][N] | No notificat | Multinacional | [281][font poc fiable?] |
| WIBP-CorV | 73% (58–82%) | 100%[E][O] | 100%[E][O] | Multinational | [273] |
| Abdala | 92% (86–96%) | No notificat | No notificat | Cuba | [282][283][font poc fiable?] |
| Soberana 02 | 62%[E] | 63%[E] | No notificat | Cuba | [284][font poc fiable?] |
| Soberana 02 i Soberana Plus | 92% (87–96%) | 100%[E] | No notificat | Cuba | |
| Novavax | 90% (75–95%) | 100%[E][O] | 100%[E][O] | United Kingdom | [285][286][287] |
| 60% (20–80%)[H] | 100%[E][O] | 100%[E][O] | Sud-àfrica | ||
| 90%[E] | No notificat | No notificat | Estats Units | ||
| No notificat | No notificat | Mèxic | |||
| CureVac | 48%[E] | No notificat | No notificat | Multinational | [288] |
| ZyCoV-D | 67%[E] | No notificat | No notificat | Índia | [289][font poc fiable?] |
| ZF2001 | 82%[E] | No notificat | No notificat | Multinational | [290][font poc fiable?] |
| SCB-2019 | 79%[E] | No notificat | No notificat | Multinational | [291] |
- ↑ Símptomes lleus: febre, tos seca, fatiga, mialgia, artràlgia, mal de coll, diarrea, nàusees, vòmits, mal de cap, anosmia, ageusia, congestió nasal, rinorrea, conjuntivitis, erupció cutània, calfreds, mareig. Símptomes moderats: pneumònia lleu.
- ↑ Els símptomes greus sense hospitalització ni la mort d'un individu són qualsevol dels següents símptomes respiratoris greus mesurats en repòs en qualsevol moment del curs de l'observació (a més de tenir pneumònia, trombosi venosa profunda, dispnea, hipòxia, dolor toràcic persistent, anorèxia, confusió, febre superior a 38ºC, però que no eren prou persistents/greus com per causar hospitalització o mort: Qualsevol freqüència respiratòria ≥ 30 respiracions/minut, freqüència cardíaca ≥ 125 pulsacions/minut, saturació d'oxigen (SpO2) ≤93% a nivell del mar, o pressió parcial d'oxigen/fracció d'oxigen inspirat (PaO2/FiO2) <300 mmHg.
- ↑ Els símptomes greus que causen hospitalització o mort són els que requereixen tractament als hospitals o produeixen morts: dispnea, hipòxia, dolor toràcic persistent, anorèxia, confusió, febre superior a 38ºC, insuficiència respiratòria, insuficiència renal, disfunció multiorgànica, sèpsia, xoc.
- ↑ Amb 12 setmanes o més d’interval entre dosis. Durant un interval inferior a 6 setmanes, l’assaig va trobar una 55% (33–70%).
- ↑ 5,00 5,01 5,02 5,03 5,04 5,05 5,06 5,07 5,08 5,09 5,10 5,11 5,12 5,13 5,14 5,15 5,16 5,17 5,18 5,19 5,20 5,21 5,22 5,23 5,24 5,25 5,26 5,27 5,28 5,29 No s'ha proporcionat un interval de confiança, de manera que no és possible conèixer la precisió d'aquesta mesura.
- ↑ Amb un interval de 4 setmanes entre dosis. L'eficàcia és "per prevenir el COVID-19 simptomàtic".
- ↑ 7,0 7,1 7,2 Els símptomes de COVID-19 observats en els assaigs de vacunes Pfizer-BioNTech només es van comptar com a tals per a les persones vacunades si van començar més de set dies després de la seva segona dosi i requerien la presència d'una RT-PCR com a resultat de la prova. Els casos lleus/moderats van requerir almenys un dels símptomes següents i una prova positiva durant els 4 dies anteriors o posteriors al període simptomàtic: febre; tos nova o augmentada; sensació de falta d'aire nova o augmentada; calfreds; dolor muscular nou o augmentat; nova pèrdua de gust o olor; mal de coll; diarrea; o vòmits. Els casos greus van requerir addicionalment almenys un dels següents símptomes: signes clínics en repòs indicatius de malaltia sistèmica greu (FR ≥30 respiracions per minut, FC ≥125 batecs per minut, SpO2 ≤93% a l'aire de l’habitació al nivell del mar o PaO2/FiO2 <300 mm Hg); insuficiència respiratòria (es defineix com la necessitat d'oxigen d’alt flux, ventilació no invasiva, ventilació mecànica o ECMO); evidència de xoc (TAS <90 mm Hg, TAD <60 mm Hg o que requereixen vasopressors); insuficiència renal aguda, hepàtica o neurològica significatives; admissió a una UCI; mort.[268]
- ↑ 8,0 8,1 8,2 8,3 Aquesta mesura no és prou precisa per donar suport a l'eficàcia elevada, ja que el límit inferior del 95% per l'interval de confiança és inferior al mínim del 30%.
- ↑ 9,0 9,1 9,2 9,3 Casos moderats.
- ↑ 10,00 10,01 10,02 10,03 10,04 10,05 10,06 10,07 10,08 10,09 10,10 10,11 L'eficàcia es va informar 28 dies després de la vacunació per a la vacuna de Janssen d'una sola administració. Es va trobar una eficàcia menor per als individus vacunats 14 dies després de la vacunació.
- ↑ 11,0 11,1 11,2 11,3 No es van detectar hospitalitzacions ni defuncions 28 dies després de la vacunació per a 19.630 persones vacunades en els assaigs, en comparació amb 16 hospitalitzacions reportades en el grup placebo de 19.691 individus (taxa d’incidència 5,2 per 1000 persones-anys)[270] i set defuncions relacionades amb la COVID-19 per al mateix grup placebo.[271]
- ↑ Els símptomes de COVID-19 lleus/moderats observats en els assaigs de vacunes Moderna, només es van comptar com a tals per a les persones vacunades si van començar més de 14 dies després de la seva segona dosi i van requerir la presència d'una PCR juntament amb almenys dos símptomes sistèmics (febre superior a 38ºC, calfreds, mialgia, mal de cap, mal de coll, trastorn olfactiu i del gust nou) o només un símptoma respiratori (tos, dificultat per respirar, o clínica o proves radiogràfiques de pneumònia).
- ↑ 13,0 13,1 Els símptomes greus de COVID-19 observats en els assaigs de vacuna Moderna es van definir com a símptomes que complien els criteris per als símptomes lleus/moderats més qualsevol de les observacions següents: Signes clínics indicatius de malaltia sistèmica greu, freqüència respiratòria ≥30 per minut, freqüència cardíaca ≥ 125 batecs per minut, SpO2 ≤93% sobre l'aire de l'habitació al nivell del mar o PaO2/FIO2 <300 mm Hg; o insuficiència respiratòria o SDRA (definida com a que necessita oxigen de flux elevat, ventilació no invasiva o mecànica o ECMO), evidència de xoc (pressió arterial sistòlica <90mmHg, TA diastòlica <60mmHg o que requereix vasopressors); o disfunció renal aguda, hepàtica o neurològica important; o ingrés en una unitat de cures intensives o defunció. No es van detectar casos greus en individus vacunats en els assaigs, en comparació amb 30 casos greus reportats en el grup amb placebo (taxa d'incidència 9,1 per cada 1000 anys-persona).
- ↑ 14,0 14,1 14,2 14,3 14,4 14,5 14,6 Aquestes dades de la fase III no s'han publicat ni revisat per especialistes.
- ↑ 15,0 15,1 15,2 15,3 15,4 15,5 No cases detected in trial.
Variants
[modifica]L'aparició potencial d'una variant SARS-CoV-2 que sigui moderadament o totalment resistent a la resposta d'anticossos provocada per l'actual generació de vacunes COVID-19 pot requerir la modificació de les vacunes.[292] Els assaigs indiquen que moltes vacunes desenvolupades per a la soca inicial tenen una eficàcia menor per a algunes variants contra la COVID-19 simptomàtica.[293] A febrer de 2021, l'FDA creia que totes les vacunes que ella va autoritzar continuaven sent efectives per protegir contra les soques circulants de SARS-CoV-2.[292]
Alfa (llinatge B.1.1.7)
[modifica]L'evidència limitada de diversos estudis preliminars revisats per l'OMS ha indicat que s'ha mantingut l'eficàcia/efectivitat contra la malaltia per l'Alfa amb les vacunes d'Oxford-AstraZeneca, Pfizer-BioNTech i Novavax, sense dades per a altres vacunes encara. És rellevant la forma en què les vacunes poden acabar amb la pandèmia evitant la infecció asimptomàtica, també indicant la conservació de la neutralització dels anticossos contra l'Alfa amb la majoria de les vacunes àmpliament distribuïdes (Sputnik V, Pfizer-BioNTech, Moderna, CoronaVac, BBIBP-CorV, Covaxin), amb una reducció mínima a moderada amb l'Oxford–AstraZeneca i encara no hi ha dades per a altres vacunes.[294]
Al desembre de 2020, es va identificar al Regne Unit una nova variant SARS-CoV-2, la variant Alfa o llinatge B.1.1.7.[295]
Els primers resultats suggereixen protecció a la variant de les vacunes Pfizer-BioNTech i Moderna.[296][297]
Un estudi va indicar que la vacuna d'Oxford-AstraZeneca tenia una eficàcia del 42-89% contra l'Alfa, enfront del 71-91% contra les altres variants.[298]
Les dades preliminars d'un assaig clínic indiquen que la vacuna Novavax és ~96% efectiva per als símptomes contra la variant original i ~86% contra l'Alfa.[299]
Beta (llinatge B.1.351)
[modifica]L'evidència limitada de diversos estudis preliminars revisats per l'OMS ha indicat una reducció de l'eficàcia/efectivitat contra les malalties per Beta amb les vacunes d'Oxford–AstraZeneca (possiblement substancial), Novavax (moderada), Pfizer-BioNTech i Janssen (mínima), sense dades per a altres vacunes encara. És rellevant la forma en què les vacunes poden acabar amb la pandèmia evitant la infecció asimptomàtica, també han indicat una neutralització dels anticossos possiblement reduïda contra la Beta amb la majoria de les vacunes àmpliament distribuïdes (Oxford–AstraZeneca, Sputnik V, Janssen, Pfizer–BioNTech, Moderna, Novavax; reducció mínima a substancial), excepte CoronaVac i BBIBP-CorV (reducció mínima a modesta), sense dades per a altres vacunes encara.[294]
Moderna ha llançat un assaig d'una vacuna per combatre la variant o llinatge Beta B.1.351.[300] Al març de 2021, Pfizer va anunciar que l'activitat de neutralització es va reduir en dos terços per a aquesta variant, tot afirmant que encara no es podien fer afirmacions definitives sobre l'eficàcia de la vacuna a l'hora de prevenir-la.[301] Diversos estudis van confirmar posteriorment la disminució de l'activitat neutralitzadora dels sèrums de pacients vacunats amb les vacunes Moderna i Pfizer-BioNTech contra la Beta.[297][302] L'1 d'abril de 2021, una actualització d'un assaig sud-africà de la de Pfizer/BioNTech va afirmar que la vacuna era 100% efectiva fins al moment (és a dir, els participants vacunats no van veure cap cas), essent la variant Beta present en sis de les nou infeccions del grup control placebo.[303]
Al gener de 2021, Johnson & Johnson o Janssen, que va realitzar assaigs per a la seva vacuna Ad26.COV2.S a Sud-àfrica, va informar que el nivell de protecció contra la infecció de moderada a severa era del 72% als Estats Units i del 57% a Sud-àfrica.[304]
El 6 de febrer de 2021, el Financial Times va informar que les dades dels assaigs provisionals d'un estudi de la Universitat sud-africana de Witwatersrand juntament amb la Universitat d'Oxford van demostrar una reducció de l'eficàcia de la vacuna Oxford-AstraZeneca contra la variant.[305] L'estudi va trobar que amb una mostra de 2.000 persones, la vacuna AZD1222 només proporcionava una "mínima protecció" en tots els casos excepte en els més greus de COVID-19.[306] El 7 de febrer de 2021, el ministre de Salut de Sud-àfrica va suspendre el desplegament previst d'un milió de dosis de la vacuna mentre examinaven les dades i esperaven consells sobre com procedir.[306][307]
Al març de 2021, es va informar que la "eficàcia preliminar" de la vacuna Novavax (NVX-CoV2373) contra la Beta per a la COVID-19 lleu, moderada o severa, per als participants amb VIH negatiu era del 51%.[308]
Gamma (llinatge P.1)
[modifica]L'evidència limitada de diversos estudis preliminars revisats per l'OMS ha indicat una eficàcia/eficiència probablement conservada contra la Gamma amb les vacunes de CoronaVac i BBIBP-CorV, sense dades per a altres vacunes encara. És rellevant la forma en què les vacunes poden acabar amb la pandèmia evitant la infecció asimptomàtica, també han indicat la conservació de la neutralització d'anticossos contra la Gamma amb les d'Oxford–AstraZeneca i CoronaVac (reducció mínima) i una neutralització lleugerament reduïda amb les de Pfizer–BioNTech i Moderna (reducció mínima a moderada), encara sense dades sobre altres vacunes.[294]
La variant Gamma o variant del llinatge P.1 (també coneguda com a 20J/501Y.V3), identificada inicialment al Brasil, sembla escapar parcialment de la vacunació amb la vacuna de Pfizer-BioNTech.[302]
Delta (llinatge B.1.617)
[modifica]L'evidència limitada de diversos estudis preliminars revisats per l'OMS ha indicat que és probable que es mantingui l'eficàcia/eficiència contra la Delta amb les vacunes d'Oxford-AstraZeneca i Pfizer-BioNTech, sense dades per a altres vacunes encara. És rellevant la forma en què les vacunes poden acabar amb la pandèmia evitant la infecció asimptomàtica, també han indicat una reducció de la neutralització dels anticossos contra la Delta amb les d'Oxford–AstraZeneca (reducció substancial), Pfizer-BioNTech i Covaxin (reducció de moderada a moderada), sense dades per a altres vacunes encara.[294]
L'octubre de 2020 es va descobrir a l'Índia una nova variant que va rebre el nom de llinatge B.1.617. Hi va haver molt poques deteccions fins al gener del 2021, però a l'abril s'havia estès a almenys 20 països de tots els continents, excepte l'Antàrtida i Amèrica del Sud.[309][310][311] Entre unes 15 mutacions definidores, té mutacions de punta D111D (sinònim), G142D, [es necessita una cita mèdica] P681R, E484Q[312] i L452R,[313] aquestes dues últimes poden fer que eviti fàcilment els anticossos.[314] La variant s'ha referit sovint com a "doble mutant", tot i que en aquest sentit no és inusual.[313] En una actualització del 15 d'abril de 2021, PHE va designar el llinatge B.1.617 com a "Variant sota investigació", VUI-21APR-01.[315] El 6 de maig de 2021, Public Health England va escalar el llinatge B.1.617.2 d'una variant sota investigació a una variant preocupant basant-se en una avaluació de la transmissibilitat que era almenys equivalent a la variant Alfa.[316]
Limitacions potencials
[modifica]El ràpid desenvolupament i la urgència de produir una vacuna per a la pandèmia COVID-19 poden augmentar els riscos i la taxa de fracàs de lliurar una vacuna segura i eficaç.[2][20][317] Un estudi va trobar que entre el 2006 i el 2015, la taxa d'èxit d'obtenir l'aprovació des de la fase I a la fase III en els assaigs va ser del 16,2% per a les vacunes,[318] i el CEPI indica una taxa d'èxit potencial del 10% només per als candidats a vacunes en el desenvolupament del 2020.[20][319][320]
Preocupació per a la bioseguretat
[modifica]Les primeres investigacions per avaluar l'eficàcia de la vacuna mitjançant models animals específics per a COVID-19, com ara ratolins transgènics ECA2, altres animals de laboratori i primats no humans, indiquen la necessitat de mesures de contenció de nivell de bioseguretat 3 per al maneig de virus vius i coordinació internacional per garantir procediments de seguretat estandarditzats.[2][20]
Potenciació per anticossos de la infecció
[modifica]Tot i que la qualitat i quantitat de producció d'anticossos per part d'una vacuna potencial està destinada a neutralitzar la infecció per COVID-19,[321] una vacuna podria tenir un efecte contrari no desitjat en provocar un augment de la malaltia dependent d'anticossos (ADE), que augmenta la fixació del virus a les seves cèl·lules diana, i llavors provocar una tempesta de citocines si més tard una persona vacunada és atacada pel virus.[2][322] La plataforma tecnològica de les vacunes (per exemple, la vacuna de vector víric, la vacuna contra la proteïna S o una subunitat proteica), la dosi de la vacuna, el moment de repetir la vacuna per una possible recurrència de la infecció per COVID-19 i l'edat avançada són factors que determinen el risc i extensió d'una possible ADE.[2][322] La resposta dels anticossos a una vacuna és una variable de les tecnologies vacunals en desenvolupament, incloent si la vacuna té precisió en el seu mecanisme,[2] i l'elecció de la ruta d'administració (intramuscular, intradèrmica, oral o nasal).[322][323]
Eficàcia
[modifica]Les mutacions del virus poden alterar la seva estructura dirigida per la vacuna, fent que la vacuna sigui ineficaç.[324][325][326] Com a exemple d'aquest últim, és poc probable que la versió mutada del virus del brot de Cluster 5, que afecta els visons a Dinamarca, respongui a les vacunes que s'estan desenvolupant actualment, segons alguns investigadors.[327] Un estudi canadenc, ara per ara pendent de revisió per experts, posa de manifest que una dosi de Vaxzevria té una efectivitat del 82% i del 87% contra l'hospitalització o la mort com a conseqüència de la infecció per les variants Beta/Gamma i Delta del virus, respectivament.[328]
Inscripció de participants en proves
[modifica]Els desenvolupadors de vacunes han d'invertir recursos a nivell internacional per trobar prou participants per a assajos clínics de fase II-III quan el virus ha demostrat ser un "objectiu en moviment" de canviar la velocitat de transmissió entre països i dins d'ells, obligant les empreses a competir pels obtenir participants en la prova.[102] Com a exemple al juny, el desenvolupador xinès de vacunes Sinovac va formar aliances amb Malàisia, Canadà, el Regne Unit i Brasil per tal de reclutar participants.[102] A mesura que la pandèmia COVID-19 a la Xina es va anar fent més aïllada i controlada, els desenvolupadors de vacunes xineses van buscar relacions internacionals per dur a terme estudis humans avançats a diversos països, creant competència per als participants de la prova amb altres fabricants i l'assaig internacional Solidaritat organitzat per l'OMS.[102] A més de la competència sobre la contractació de participants, els organitzadors d'assaigs clínics poden trobar-se amb persones que no vulguin vacunar-se a causa d'estar-hi en contra[329] o al no creure en la ciència de la tecnologia de la vacuna i en la seva capacitat per prevenir la infecció.[330]
Tenir un nombre insuficient de membres de l'equip qualificat per administrar les vacunes pot dificultar els assajos clínics que han de superar els riscos de fracàs de l'assaig, com ara el reclutament de participants en regions geogràfiques rurals o de baixa densitat, i les variacions d'edat, raça, ètnia o afeccions mèdiques subjacents.[102][331]
Refús a les vacunes
[modifica]Al voltant del 10% del públic percep les vacunes com a insegures o innecessàries, rebutjant la vacunació,[332][333] fet que augmenta el risc de propagació viral addicional que podria provocar brots de COVID-19.[329] A mitjan 2020, les estimacions de dues enquestes indicaven que el 67% o el 80% de les persones als Estats Units acceptaria una nova vacuna contra la COVID-19, amb una gran disparitat per nivell d'educació, estat laboral, raça i geografia.[334][335]
Una enquesta duta a terme per National Geographic i Morning Consult va demostrar una bretxa de gènere en la intenció de prendre una vacuna COVID-19 als EUA, amb un 69% dels homes enquestats que prendrien la vacuna, en comparació amb només el 51% de les dones. L'enquesta també va mostrar una correlació positiva entre el nivell educatiu i la voluntat de prendre la vacuna.[336]
Segons un estudi multicèntric fet als EUA, 182 milions d'habitants del país estaven completament vacunats contra la COVID-19, amb dosis de Pfizer-BioNTech (BNT162b2), Moderna (mRNA-1273) i Janssen (Johnson & Johnson; Ad.26.COV2.S) a finals de setembre de 2021. Encara que els receptors de les vacunes tingueren taxes de mortalitat no relacionades amb la malaltia menors que les de les persones no vacunades, després d'ajustar les dades per edat, sexe, raça i etnicitat i lloc del estudi es va observar que el nombre de vacunacions diàries havia disminuït un 78% des de mitjans d'abril del mateix any, un fet que els investigadors atribuïren a un augment generalitzat de les dubtes sobre la seva eficàcia.[337]
Cost
[modifica]Una vacuna eficaç contra la COVID-19 podria estalviar bilions de dòlars en impacte econòmic mundial i, per tant, faria que qualsevol preu dels milers de milions resultés petit en comparació.[338] En les primeres etapes de la pandèmia, no se sabia si seria possible crear una vacuna segura, fiable i assequible per a aquest virus, i no se sabia exactament quant podia costar el desenvolupament de la vacuna.[19][319][339] Hi havia la possibilitat que es poguessin invertir milers de milions de dòlars sense èxit.[340]
Un cop es desenvolupés una vacuna eficaç, caldria fabricar i distribuir milers de milions de dosis a tot el món. A l'abril de 2020, la Fundació Gates va estimar que la fabricació i la distribució podrien costar fins a 25.000 milions de dòlars EUA.[341] El 4 de maig de 2020, la Comissió Europea va organitzar i va celebrar una videoconferència de líders mundials en què es van recaptar 8.000 milions de dòlars EUA per al desenvolupament de la vacuna COVID-19.[342]
Al novembre de 2020, les empreses subvencionades en el marc del programa Operation Warp Speed dels Estats Units han fixat un preu inicial entre 19,50 i 25 dòlars EUA per dosi, en línia amb la vacuna antigripal.[343]
El desembre de 2020, una política belga va publicar breument els preus confidencials acordats entre els productors de vacunes i la Unió Europea:[344]
| Fabricant | Preu per dosi a la UE[345] |
|---|---|
| AstraZeneca | 1,78 € |
| Janssen | 8,50$ |
| Sanofi/GSK | 7,56 € |
| Pfizer/BioNTech | 12,00 € |
| Curevac | 10,00 € |
| Moderna | 18,00$ |
Distribució
[modifica]Les diferents vacunes tenen requisits d'enviament i manipulació diferents. Per exemple, la vacuna de Pfizer/BioNTech tozinameran s'ha d'enviar i emmagatzemar entre −80 i −60 °C,[346] s'ha d'utilitzar en un termini de cinc dies de descongelació,[346] i té un ordre mínim de 975 dosis, pel que és poc probable que es distribueixi en entorns diferents al que són els entorns de grans hospitals ben equipats.[347] Els vials de vacunes de Moderna requereixen emmagatzematge a més de -40 °C i una refrigeració entre -25 i -15 °C en la distribució. Un cop refrigerada, la vacuna Moderna COVID-19 es pot mantenir entre 2 i 8 °C durant un màxim de 30 dies.[348]
Manca de dades públiques i confiança
[modifica]Per exemple, l'aprovació dels Emirats Àrabs Units de la vacuna xinesa BBIBP-CorV es feu amb manca notable de dades i altres detalls crítics.[349] A diferència de les vacunes que es desenvolupen en alguns països occidentals, hi ha poca informació pública sobre la seguretat o l'eficàcia de les vacunes xineses.[350] Tot i que els Emirats Àrabs Units van dir que havien revisat les dades de Sinopharm en una anàlisi provisional, no hi havia cap indicació que s'hagués analitzat de manera independent les dades en brut. No està clar com Sinopharm va treure conclusions de les dades, ja que els Emirats Àrabs Units no van indicar detalls crítics de l'anàlisi, com ara el nombre de casos de COVID-19 o l'edat dels voluntaris.[349] Zhengming Chen, epidemiòleg de la Universitat d'Oxford, va dir: "És difícil saber fins a quin punt funciona la vacuna. Espero que sigui real".[351]
Desinformació
[modifica]A principis de 2020, les publicacions a les xarxes socials promogueren una teoria conspiratòria segons la qual una vacuna contra la COVID-19 ja estava disponible. Les patents citades per diverses publicacions en aquests mitjans de comunicació feien referència a patents existents per a seqüències genètiques i vacunes per a altres soques de coronavirus com el SARS-CoV, però no per a la causant de la COVID-19.[352][353] A mitjans de juliol de 2021, amb menys de la meitat de la seva població vacunada, les autoritats sanitàries dels EUA publicaren un comunicat que qualificava a la desinformació de greu perill per la salut pública nacional.[354] Amb l'objectiu de detectar automàticament la desinformació relacionada amb les vacunes contra la COVID-19, experts informàtics dels EUA han desenvolupat un mètode experimental basat en la predicció d'enllaços en gràfics.[355]
Referències
[modifica]- ↑ «A l'entorn del coronavirus». Termcat, 12-02-2020. [Consulta: 23 març 2020].
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 2,7 Diamond, Michael S; Pierson, Theodore C «The challenges of vaccine development against a new virus during a pandemic» (en anglès). Cell Host and Microbe, 27, 5, 13-05-2020, pp: 699–703. DOI: 10.1016/j.chom.2020.04.021. PMC: 7219397. PMID: 32407708.
- ↑ Padilla, Teodoro B. «No one is safe unless everyone is safe» (en anglès). Medicine Cabinet, BusinessWorld, 24-02-2021 [Consulta: 30 març 2021].
- ↑ Branswell, Helen. «A side-by-side comparison of the Pfizer/BioNTech and Moderna vaccines» (en anglès). Stat News, 19-12-2020. [Consulta: 30 març 2021].[Enllaç no actiu]
- ↑ 5,0 5,1 5,2 5,3 Vaccine Centre. «COVID-19 vaccine tracker» (en anglès). London School of Hygiene and Tropical Medicine, 11 juliol 2021 (rev). [Consulta: 11 juliol 2021].
- ↑ «Zydus Cadila: India approves world's first DNA Covid vaccine», 20-08-2021. [Consulta: 5 agost 2022].
- ↑ (23 August 2021). "FDA Approves First COVID-19 Vaccine". Nota de premsa.
- ↑ (17 June 2022). "Coronavirus (COVID-19) Update: FDA Authorizes Moderna and Pfizer-BioNTech COVID-19 Vaccines for Children Down to 6 Months of Age". Nota de premsa.
- ↑ «China's Sixth Covid-19 Vaccine Is Approved for Emergency Use», 09-06-2021. [Consulta: 5 agost 2022].
- ↑ Beaumont, Peter «Covid-19 vaccine: who are countries prioritising for first doses?» (en anglès). The Guardian. ISSN 0261-3077, 18-11-2020 [Consulta: 26 desembre 2020].
- ↑ Plotkin, SA; Halsey, N «Accelerate COVID-19 Vaccine Rollout by Delaying the Second Dose of mRNA Vaccines» (en anglès). Clinical Infectious Diseases, 2021; Gen 27, pp: ciab068. DOI: 10.1093/cid/ciab068. PMC: 7929065. PMID: 33502467 [Consulta: 11 juliol 2021].
- ↑ Epperly, DE «Evidence For COVID-19 Vaccine Deferred Dose 2 Boost Timing» (en anglès). Social Science Research Network Electronic Journal, 2021; Gen 5, pàgs: 1-7. DOI: 10.2139/ssrn.3760833. ISSN: 1556-5068 [Consulta: 29 juny 2021].[Enllaç no actiu]
- ↑ Wang, X «Safety and Efficacy of the BNT162b2 mRNA Covid-19 Vaccine» (en anglès). N Engl J Med, 384, 11, 22-04-2021, pp: 1577-1578. DOI: 10.1056/NEJMc2036242. ISSN: 1533-4406. PMID: 33596350 [Consulta: 2 octubre 2021].
- ↑ Really Correct™. «More Evidence: Evidence For COVID-19 Vaccine Deferred Dose 2 Boost Timing» (en anglès). COVID-19 Topics, 17-02-2021. [Consulta: 14 octubre 2021].
- ↑ Ritchie, Hannah; Ortiz-Ospina, Esteban; Beltekian, Diana; Mathieu, Edouard; Hasell, Joe; et al «Coronavirus Pandemic (COVID-19)» (en anglès). Our World in Data, 05-08-2021 [Consulta: 6 agost 2021].
- ↑ Mullard, Asher «How COVID vaccines are being divvied up around the world. Canada leads the pack in terms of doses secured per capita» (en anglès). Nature News, 30-11-2020. DOI: 10.1038/d41586-020-03370-6. ISSN: 1476-4687. PMID: 33257891 [Consulta: 11 desembre 2020].
- ↑ So, Anthony D.; Woo, Joshua «Reserving coronavirus disease 2019 vaccines for global access: cross sectional analysis» (en anglès). BMJ, 2020; Des 15; 371, pp: m4750. DOI: 10.1136/bmj.m4750. ISSN: 1756-1833. PMID: 33323376 [Consulta: 8 juliol 2021].
- ↑ 18,0 18,1 18,2 18,3 18,4 18,5 Le TT, Cramer JP, Chen R, Mayhew S «Evolution of the COVID-19 vaccine development landscape» (en anglès). Nature Reviews. Drug Discovery, 19, 10, 07-09-2020, pp: 667–668. DOI: 10.1038/d41573-020-00151-8. ISSN: 1474-1784. PMID: 32887942.
- ↑ 19,0 19,1 19,2 Gates, Bill. «The vaccine race explained: What you need to know about the COVID-19 vaccine» (en anglès). The Gates Notes, 30-04-2020. [Consulta: 2 maig 2020].
- ↑ 20,0 20,1 20,2 20,3 20,4 20,5 Thanh Le, Tung; Andreadakis, Zacharias; Kumar, Arun; Gómez Román, Raúl; Tollefsen, Stig; Saville, Melanie; Mayhew, Stephen «The COVID-19 vaccine development landscape» (en anglès). Nature Reviews Drug Discovery, 19, 5, 09-04-2020, pp: 305–306. DOI: 10.1038/d41573-020-00073-5. ISSN: 1474-1776. PMID: 32273591.
- ↑ Klass, P; Ratner, AJ «Vaccinating Children against Covid-19 - The Lessons of Measles» (en anglès). N Engl J Med, 2021 Feb 18; 384 (7), pp: 589-591. DOI: 10.1056/NEJMp2034765. ISSN: 1533-4406. PMID: 33471977 [Consulta: 15 agost 2021].
- ↑ Krammer, F «SARS-CoV-2 vaccines in development» (en anglès). Nature, 586, 7830, 10-2020, pp: 516–527. DOI: 10.1038/s41586-020-2798-3. ISSN: 1476-4687. PMID: 32967006.
- ↑ Park KS, Sun X, Aikins ME, Moon JJ «Non-viral COVID-19 vaccine delivery systems» (en anglès). Advanced Drug Delivery Reviews, 169, 17-12-2020, pp: 137–151. DOI: 10.1016/j.addr.2020.12.008. PMC: 7744276. PMID: 33340620 [Consulta: 15 agost 2021].
- ↑ Kowalski PS, Rudra A, Miao L, Anderson DG «Delivering the Messenger: Advances in Technologies for Therapeutic mRNA Delivery» (en anglès). Mol Ther, 27, 4, 10-04-2019, pp: 710–728. DOI: 10.1016/j.ymthe.2019.02.012. PMC: 6453548. PMID: 30846391.
- ↑ Verbeke R, Lentacker I, De Smedt SC, Dewitte H «Three decades of messenger RNA vaccine development» (en anglès). Nano Today, 28, 10-2019, pp: 100766. DOI: 10.1016/j.nantod.2019.100766. ISSN: 1748-0132.
- ↑ Advisory Committee on Immunization Practices. «COVID-19 ACIP Vaccine Recommendations» (en anglès). Centers for Disease Control and Prevention (CDC), 30 agost 2021 (rev). [Consulta: 2 setembre 2021].
- ↑ European Commission. «Safe COVID-19 vaccines for Europeans» (en anglès). Coronavirus response, 31 agost 2021 (rev). [Consulta: 2 setembre 2021].
- ↑ 28,0 28,1 Palca, Joe. «Scientists Race to Develop Next Generation of COVID Vaccines», 06-04-2021.
- ↑ 29,0 29,1 European Medicines Agency (EMA) «EMA starts rolling review of CureVac's COVID-19 vaccine (CVnCoV)» (en anglès). Press office, 12-02-2020 [Consulta: 12 febrer 2021].
- ↑ Nilsson, L; Csuth, À; Storsaeter, J; Garvey, LH; Jenmalm, MC «Vaccine allergy: evidence to consider for COVID-19 vaccines» (en anglès). Curr Opin Allergy Clin Immunol, 2021 Ag 1; 21 (4), pp: 401-409. DOI: 10.1097/ACI.0000000000000762. PMC: 8270228. PMID: 34091550.
- ↑ 31,0 31,1 31,2 Moghimi, SM «Allergic Reactions and Anaphylaxis to LNP-Based COVID-19 Vaccines» (en anglès). Molecular Therapy, 29, 3, 2021; Mar 3, pp: 898–900. DOI: 10.1016/j.ymthe.2021.01.030. PMC: 7862013. PMID: 33571463.
- ↑ 32,0 32,1 Gavi: The Vaccine Alliance. «What are viral vector-based vaccines and how could they be used against COVID-19?» (en anglès). News & Resources, 2020; Des 18. [Consulta: 26 gener 2021].
- ↑ CDC. «Understanding Viral Vector COVID-19 Vaccines» (en anglès). NCIRD, Division of Viral Diseases. US Department of Health & Human Services, 13-04-2021. [Consulta: 19 abril 2021].
- ↑ Johnson, Carolyn Y.; McGinley, Laurie «Johnson & Johnson seeks emergency FDA authorization for single-shot coronavirus vaccine» (en anglès). Health, The Washington Post, 05-02-2021.
- ↑ McGregor, Grady. «It’s not just Johnson & Johnson: China has a single-dose COVID-19 vaccine that’s 65% effective» (en anglès). Fortune, 09-02-2021. [Consulta: 28 febrer 2021].
- ↑ Wu S, Zhong G, Zhang J, Shuai L, Zhang Z, Wen Z, Wang B, Zhao Z, Song X, et al «A single dose of an adenovirus-vectored vaccine provides protection against SARS-CoV-2 challenge» (en anglès). Nat Commun, 11, 1, 14-08-2020, pàg. 4081. DOI: 10.1038/s41467-020-17972-1. PMC: 7427994. PMID: 32796842.
- ↑ Sanders, B; Koldijk, M; Schuitemaker, H «Inactivated Viral Vaccines» (en anglès). A: Nature Public Health Emergency Collection - Vaccine Analysis: Strategies, Principles, and Control, 2014; Nov 28, pp: 45–80. DOI: 10.1007/978-3-662-45024-6_2. PMC: 7189890 [Consulta: 3 octubre 2021].
- ↑ Petrovsky, Nikolai; Aguilar, Julio César «Vaccine adjuvants: Current state and future trends» (en anglès). Immunology and Cell Biology, 82, 5, 28-09-2004, pp: 488–496. DOI: 10.1111/j.0818-9641.2004.01272.x. ISSN: 0818-9641. PMID: 15479434.
- ↑ Ivanova, Polina. «Russia approves its third COVID-19 vaccine, CoviVac» (en anglès). Reuters, 20-02-2021. [Consulta: 11 abril 2021].
- ↑ Staff. «Kazakhstan rolls out its own COVID-19 vaccine» (en anglès). Reuters, 27-04-2021. [Consulta: 2 juliol 2021].
- ↑ Carlson, Robert; Lutmer, Holly & Staff. «VLA2001 COVID-19 Vaccine» (en anglès). Precision Vaccinations, 11 agost 2020 (rev). [Consulta: 15 agost 2021].
- ↑ Valneva Clinical Development (Valneva Austria GmbH). «Dose Finding Study to Evaluate Safety, Tolerability and Immunogenicity of an Inactiviated Adjuvanted Sars-Cov-2 Virus Vaccine Candidate Against Covid-19 in Healthy Adults» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 17 desembre 2020; IDNCT04671017. [Consulta: 15 agost 2021].
- ↑ Mekonnen, D; Mengist, HM; Jin, T «SARS-CoV-2 subunit vaccine adjuvants and their signaling pathways» (en anglès). Expert review of vaccines, 2021; Nov 1, pp: 1-13. DOI: 10.1080/14760584.2021.1991794. PMC: 8567292. PMID: 34633259 [Consulta: 17 desembre 2021].
- ↑ WHO. «MODULE 2 – Types of Vaccine and Adverse Reactions: Subunit vaccines» (en anglès). Vaccine Safety Basics, e-learning course. Arxivat de l'original el 2021-03-20. [Consulta: 21 gener 2021].
- ↑ Kuzubov, Vladimir I. (Federal Budgetary Research Institution State Research Center of Virology and Biotechnology "Vector"). «Study of the Safety, Reactogenicity and Immunogenicity of "EpiVacCorona" Vaccine for the Prevention of COVID-19 (EpiVacCorona)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 22 setembre 2020; IDNCT04527575. [Consulta: 30 març 2021].
- ↑ The University of Queensland. «A Study on the Safety, Tolerability and Immune Response of SARS-CoV-2 Sclamp (COVID-19) Vaccine in Healthy Adults» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 3 agost 2020; IDNCT04495933. [Consulta: 4 agost 2020].
- ↑ «UQ-CSL V451 Vaccine». Arxivat de l'original el 19 de desembre 2020. [Consulta: 11 desembre 2020].
- ↑ 48,0 48,1 «Safety, Tolerability and Immunogenicity of INO-4800 for COVID-19 in Healthy Volunteers». United States National Library of Medicine, 07-04-2020. Arxivat de l'original el 11 octubre 2020.
- ↑ 49,0 49,1 «IVI, INOVIO, and KNIH to partner with CEPI in a Phase I/II clinical trial of INOVIO's COVID-19 DNA vaccine in South Korea». International Vaccine Institute, 16-04-2020.
- ↑ 50,0 50,1 Clinical Development Team (AnGes, Inc.). «Study of COVID-19 DNA Vaccine (AG0301-COVID19)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 9 juliol 2020; IDNCT04463472. [Consulta: 14 juliol 2020].
- ↑ Woo, JungWon (Genexine, Inc.). «Safety and Immunogenicity Study of GX-19, a COVID-19 Preventive DNA Vaccine in Healthy Adults» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 24 juny 2020; IDNCT04445389. [Consulta: 14 juliol 2020].
- ↑ Staff «S. Korea's Genexine begins human trial of coronavirus vaccine» (en anglès). Reuters, 19-06-2020 [Consulta: 25 juny 2020].
- ↑ Chang, Lung-Ji (Shenzhen Geno-Immune Medical Institute). «Safety and Immunity of Covid-19 aAPC Vaccine» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 9 març 2020; IDNCT04299724. [Consulta: 14 juliol 2020].
- ↑ Chang, Lung-Ji (Shenzhen Geno-Immune Medical Institute). «Immunity and Safety of Covid-19 Synthetic Minigene Vaccine» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 19 febrer 2020; IDNCT04276896. [Consulta: 14 juliol 2020].
- ↑ Israel Institute for Biological Research (IIBR). «A Phase I/II Randomized, Multi-Center, Placebo-Controlled, Dose-Escalation Study to Evaluate the Safety, Immunogenicity and Potential Efficacy of an rVSV-SARS-CoV-2-S Vaccine (IIBR-100) in Adults» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 1 novembre 2020; IDNCT04608305.
- ↑ Johnson, Carolyn Y.; Mufson, Steven «Can old vaccines from science's medicine cabinet ward off coronavirus?» (en anglès). The Washington Post ISSN 0190-8286 [Consulta: 31 desembre 2020].
- ↑ World Health Organization (WHO). «Bacille Calmette-Guérin (BCG) vaccination and COVID-19» (en anglès)). Scientific brief, 12-04-2020. [Consulta: 1r maig 2020].
- ↑ Gong, W; Aspatwar, A; Wang, S; Parkkila, S; Wu, X «COVID-19 pandemic: SARS-CoV-2 specific vaccines and challenges, protection via BCG trained immunity, and clinical trials» (en anglès). Expert Rev Vaccines, 2021 Jul; 20 (7), pp: 857-880. DOI: 10.1080/14760584.2021.1938550. PMC: 8220438. PMID: 34078215 [Consulta: 4 novembre 2021].
- ↑ 59,0 59,1 Tregoning JS, Russell RF, Kinnear E «Adjuvanted influenza vaccines» (en anglès). Human Vaccines & Immunotherapeutics, 14, 3, 04-03-2018, pp: 550–564. DOI: 10.1080/21645515.2017.1415684. PMC: 5861793. PMID: 29232151.
- ↑ 60,0 60,1 60,2 60,3 Wang J, Peng Y, Xu H, Cui Z, Williams RO «The COVID-19 Vaccine Race: Challenges and Opportunities in Vaccine Formulation» (en anglès). AAPS PharmSciTech, 21, 6, 05-08-2020, pp: 225. DOI: 10.1208/s12249-020-01744-7. PMC: 7405756. PMID: 32761294.
- ↑ Liang, Z; Zhu, H; Wang, Y; Jing, B; et al «Adjuvants for Coronavirus Vaccines» (en anglès). Front Immunol, 2020 Nov 6; 11, pp: 589833. DOI: 10.3389/fimmu.2020.589833. PMC: 7677582. PMID: 33240278.
- ↑ Simpson S, Kaufmann MC, Glozman V, Chakrabarti A «Disease X: accelerating the development of medical countermeasures for the next pandemic» (en anglès). The Lancet. Infectious Diseases, 2020 Maig; 20 (5), pp: e108–e115. DOI: 10.1016/S1473-3099(20)30123-7. PMC: 7158580. PMID: 32197097.
- ↑ 63,0 63,1 Our World in Data. «Coronavirus (COVID-19) Vaccinations» (en anglès). Statistics and Research, 17-02-2020. [Consulta: 19 febrer 2020].
- ↑ «World Health Organization timeline – COVID-19». World Health Organization, 27-04-2020. Arxivat de l'original el 29 abril 2020.
- ↑ 65,0 65,1 65,2 Thanh Le, Tung; Andreadakis, Zacharias; Kumar, Arun; Gómez Román, Raúl; Tollefsen, Stig; Saville, Melanie; Mayhew, Stephen «The COVID-19 vaccine development landscape». Nature Reviews Drug Discovery, 19, 5, 09-04-2020, pàg. 305–06. DOI: 10.1038/d41573-020-00073-5. ISSN: 1474-1776. PMID: 32273591.
- ↑ 66,0 66,1 «Responding to Covid-19: A once-in-a-century pandemic?». The New England Journal of Medicine, 382, 18, 2-2020, pàg. 1677–79. DOI: 10.1056/nejmp2003762. PMID: 32109012.
- ↑ «Covid-19: Navigating the uncharted». The New England Journal of Medicine, 382, 13, 3-2020, pàg. 1268–69. DOI: 10.1056/nejme2002387. PMC: 7121221. PMID: 32109011.
- ↑ 68,0 68,1 Le, Tung Thanh; Cramer, Jakob P.; Chen, Robert; Mayhew, Stephen «Evolution of the COVID-19 vaccine development landscape». Nature Reviews Drug Discovery, 19, 10, 04-09-2020, pàg. 667–68. DOI: 10.1038/d41573-020-00151-8. ISSN: 1474-1776. PMID: 32887942.
- ↑ ; Yadav, Prashant; Berkley, Seth «A COVID-19 vaccine will need equitable, global distribution». Harvard Business Review, 02-04-2020.
- ↑ «COVID-19 pandemic reveals the risks of relying on private sector for life-saving vaccines, says expert». CBC Radio, 08-05-2020.
- ↑ Ahmed, Darius D. «Oxford, AstraZeneca COVID-19 deal reinforces 'vaccine sovereignty'». Stat, 04-06-2020. Arxivat de l'original el 12 juny 2020.
- ↑ ; Drew, Trevor«Here's why the WHO says a coronavirus vaccine is 18 months away», 14-02-2020.
- ↑ «Update on WHO Solidarity Trial – Accelerating a safe and effective COVID-19 vaccine». World Health Organization, 27-04-2020. Arxivat de l'original el 30 abril 2020. «És vital que avaluem tantes vacunes com sigui possible, ja que no podem predir quantes resultaran ser viables. Per augmentar les possibilitats d’èxit (donat l¡elevat nivell de desgast durant el desenvolupament de la vacuna), hem de provar totes les vacunes candidates fins que fallin. [L'OMS] treballa per garantir que tots puguin tenir proves en la fase inicial del desenvolupament. Els resultats sobre l'eficàcia de cada vacuna s'esperen en un termini de tres a sis mesos i aquesta evidència, combinada amb dades sobre seguretat, informarà les decisions sobre si es pot utilitzar a una escala més àmplia..»
- ↑ «Ensuring global access to COVID‑19 vaccines». Lancet, 395, 10234, 5-2020, pàg. 1405–06. DOI: 10.1016/S0140-6736(20)30763-7. PMC: 7271264. PMID: 32243778. «CEPI estima desenvolupar fins a tres vacunes en els propers 12-18 mesos requerirà una inversió d'almenys 2.000 milions de dòlars EUA. Aquesta estimació inclou assajos clínics de fase I de vuit candidats a vacunes, progressió de fins a sis candidats mitjançant assaigs de fase II i III, finalització de requisits reguladors i de qualitat per a almenys tres vacunes i millora de la capacitat de fabricació mundial de tres vacunes.»
- ↑ «WHO 'backed China's emergency use' of experimental Covid-19 vaccines», 25-09-2020. Arxivat de l'original el 26 setembre 2020.
- ↑ Kramer, Andrew E. «Russia Is Slow to Administer Virus Vaccine Despite Kremlin's Approval». The New York Times, 19-09-2020.
- ↑ (20 novembre 2020). "Pfizer and BioNTech to Submit Emergency Use Authorization Request Today to the U.S. FDA for COVID-19 Vaccine". Nota de premsa.
- ↑ Park, Alice «Exclusive: Pfizer CEO Discusses Submitting the First COVID-19 Vaccine Clearance Request to the FDA». Time, 20-11-2020.
- ↑ «Information for Healthcare Professionals on Pfizer/BioNTech COVID-19 vaccine», 08-12-2020.
- ↑ «Conditions of Authorisation for Pfizer/BioNTech COVID-19 vaccine», 03-12-2020.
- ↑ «UK medicines regulator gives approval for first UK COVID-19 vaccine». Medicines and Healthcare Products Regulatory Agency, Government of the UK, 02-12-2020.
- ↑ «U.K. Approves Pfizer Coronavirus Vaccine, a First in the West». The New York Times, 02-12-2020.
- ↑ Roberts, Michelle «Covid Pfizer vaccine approved for use next week in UK». BBC, 02-12-2020.
- ↑ «Questions and Answers: COVID-19 vaccination in the EU», 21-12-2020.
- ↑ «Bahrain second in the world to approve the Pfizer/BioNTech Covid-19 vaccine». Bahrain News Agency, 04-12-2020.
- ↑ «UAE: Ministry of Health announces 86 per cent vaccine efficacy». Gulf News.
- ↑ ; LaFraniere, Sharon; Weiland, Noah; Goodnough, Abby; Haberman, Maggie «F.D.A. Clears Pfizer Vaccine, and Millions of Doses Will Be Shipped Right Away». The New York Times, 12-12-2020.
- ↑ "FDA Takes Additional Action in Fight Against COVID-19 By Issuing Emergency Use Authorization for Second COVID-19 Vaccine". Nota de premsa.
- ↑ Oliver, Sara E.; Gargano, Julia W.; Marin, Mona; Wallace, Megan; Curran, Kathryn G.; Chamberland, Mary; McClung, Nancy; Campos-Outcalt, Doug; Morgan, Rebecca L. «The Advisory Committee on Immunization Practices' Interim Recommendation for Use of Moderna COVID-19 Vaccine — United States, December 2020». MMWR. Morbidity and Mortality Weekly Report, 69, 5152, 12-2020, pàg. 1653–1656. DOI: 10.15585/mmwr.mm695152e1. PMID: 33382675.
- ↑ «FDA approves second Covid vaccine for emergency use as it clears Moderna's for U.S. distribution». CNBC, 19-12-2020.
- ↑ Caddy, S «Russian SARS-CoV-2 vaccine» (en anglès). BMJ, 2020 Ag 24; 370, pp: m3270. ISSN 1756-1833. DOI: 10.1136/bmj.m3270. PMID: 32839191 [Consulta: 7 febrer 2021].
- ↑ Balakrishnan, VS «The arrival of Sputnik V» (en anglès). Lancet Infect Dis, 2020 Oct; 20 (10), pp: 1128. PMID: 32979327. DOI: 10.1016/S1473-3099(20)30709-X. PMC: 7511201 [Consulta: 3 febrer 2021].
- ↑ Logunov, DY; Dolzhikova, IV; Shcheblyakov, DV; Tukhvatulin, AI; et al «Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia» (en anglès). Lancet, 2021; Feb 2, pàgs: 15. ISSN 1474-547X. DOI: 10.1016/S0140-6736(21)00234-8 [Consulta: 3 febrer 2021].
- ↑ «Russia registers world's first COVID-19 vaccine for animals» (en anglès). Reuters, 31-03-2021.
- ↑ «В России зарегистрировали первую в мире вакцину против COVID-19 для животных» (en russian). TASS [Moscow], 31-03-2021.
- ↑ «EXCLUSIVE Blackwater founder Prince takes role in COVID vaccine venture», 04-06-2021. [Consulta: 4 juny 2021].
- ↑ Hipra. «Vacuna COVID-19: Estem investigant una nova vacuna contra la Covid-19», 2021. [Consulta: 21 abril 2021].
- ↑ Puntí, Joan. «Hipra començarà els assaigs clínics de la seva vacuna contra la Covid al juny». Salut, El Punt Avui, 25-02-2021. [Consulta: 21 abril 2021].
- ↑ Duran, Xavier. «Can Ruti, primer centre de l'estat que assajarà una vacuna pròpia contra la Covid». Notícies; CCMA, SA, 31-10-2020. [Consulta: 21 abril 2021].
- ↑ 100,0 100,1 CDC. «Safety of COVID-19 Vaccines» (en anglès). NCIRD, Division of Viral Diseases. US Department of Health and Human Services, 1 novembre 2021 (rev). [Consulta: 4 novembre 2021].
- ↑ 101,0 101,1 101,2 United States Food and Drug Administration (FDA). «The drug development process» (en anglès). Learn About Drug and Device Approvals, 04-01-2018. [Consulta: 12 abril 2020].
- ↑ 102,0 102,1 102,2 102,3 102,4 Cohen, Jon «Pandemic vaccines are about to face the real test» (en anglès). Science, 368, 6497, 19-06-2020, pp: 1295–1296. DOI: 10.1126/science.368.6497.1295. ISSN: 1095-9203. PMID: 32554572.
- ↑ «How flu vaccine effectiveness and efficacy are measured». Centers for Disease Control and Prevention, National Center for Immunization and Respiratory Diseases, US Department of Health and Human Services, 29-01-2016. Arxivat de l'original el 7 maig 2020. [Consulta: 6 maig 2020].
- ↑ «Principles of epidemiology, Section 8: Concepts of disease occurrence». Centers for Disease Control and Prevention, Center for Surveillance, Epidemiology, and Laboratory Services, US Department of Health and Human Services, 18-05-2012. Arxivat de l'original el 6 abril 2020. [Consulta: 6 maig 2020].
- ↑ 105,0 105,1 Pallmann P, Bedding AW, Choodari-Oskooei B, Dimairo M, Flight L, Hampson LV, Holmes J, et al «Adaptive designs in clinical trials: why use them, and how to run and report them» (en anglès). BMC Medicine, 16, 1, 28-02-2018, pp: 29. DOI: 10.1186/s12916-018-1017-7. PMC: 5830330. PMID: 29490655.
- ↑ Food and Drug Administration (FDA). «Adaptive designs for clinical trials of drugs and biologics: Guidance for industry» (en anglès). Center for Drug Evaluation and Research/Center for Biologics Evaluation and Research, US Department of Health and Human Services, 01-11-2019. [Consulta: 3 abril 2020].
- ↑ «An international randomised trial of candidate vaccines against COVID-19: Outline of Solidarity vaccine trial». World Health Organization (WHO), 09-04-2020. Arxivat de l'original el 12 maig 2020. [Consulta: 9 maig 2020].
- ↑ «Urgent global health needs addressed by Novavax». Novavax. Arxivat de l'original el 12 de maig de 2021. [Consulta: 30 gener 2021].
- ↑ «COVID-19 vaccine tracker (Refresh URL to update)». London School of Hygiene & Tropical Medicine, 12-07-2021. [Consulta: 10 març 2021].
- ↑ Milken Institute. «COVID-19 vaccine tracker (Choose vaccines tab, apply filters to view select data)» (en angles). FasterCures, 26 agost 2021 (rev). [Consulta: 29 agost 2021].
- ↑ R&D Blueprint team. «Draft landscape of COVID 19 candidate vaccines» (en anglès). World Health Organization, 10-12-2020. [Consulta: 11 desembre 2020].
- ↑ Sanofi Pasteur, GlaxoSmithKline. «Study of Monovalent and Bivalent Recombinant Protein Vaccines Against COVID-19 in Adults 18 Years of Age and Older (VAT00008)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 27-05-2021. [Consulta: 28 maig 2021].
- ↑ WHO. «Study of Recombinant Protein Vaccine with Adjuvant against COVID-19 in Adults 18 Years of Age and Older» (en anglès). ICTRP Search Portal, 30 agost 2021 (rev). [Consulta: 20 octubre 2021].
- ↑ «Tarjeta del participante del estudio VAT00008: ejemplo central para adaptación a nivel de país» (en castellà). Instituto Nacional Salvador Zubirán de Ciencias de la Salud y Nutrición, 15-04-2021.
- ↑ Sanofi Pasteur/GlaxoSmithKline. «Study of Recombinant Protein Vaccine Formulations Against COVID-19 in Healthy Adults 18 Years of Age and Older» (en anglès). Clinicaltrials.gov, United States National Library of Medicine. [Consulta: 11 març 2021].
- ↑ Sanofi Pasteur/GlaxoSmithKline. «Study of Recombinant Protein Vaccine With Adjuvant Against COVID-19 in Adults 18 Years of Age and Older (VAT00002)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 21 febrer 2021; IDNCT04762680. [Consulta: 11 març 2021].
- ↑ GlaxoSmithKline plc. «Sanofi and GSK sign agreements with the Government of Canada to supply up to 72 million doses of adjuvanted COVID-19 vaccine» (en anglès britànic). Press releases, 22-09-2020. [Consulta: 1r abril 2021].
- ↑ Paton, J; Griffin, R; Koons, C «Prognosis: U.S. Likely to Get Sanofi Vaccine First If It Succeeds» (en anglès). Bloomberg L.P, 13-05-2020 [Consulta: 1r abril 2021].
- ↑ BBC News «Coronavirus vaccine: UK signs deal with GSK and Sanofi» (en anglès). Business, 29-07-2020 [Consulta: 24 agost 2021].
- ↑ GSK. «Sanofi and GSK confirm agreement with European Union to supply up to 300 million doses of adjuvanted COVID-19 vaccine» (en anglès britànic). Press releases, 18-09-2020. [Consulta: 1r abril 2021].
- ↑ «VN starts injection of homegrown COVID-19 vaccine in first-stage human trial». Viet Nam News, 17-12-2020.
- ↑ WHO. «Draft landscape and tracker of COVID-19 candidate vaccines» (en anglès). R&D Blueprint team, 10 desembre 2021 (rev). [Consulta: 11 desembre 2021].
- ↑ «How much does first Made-in Vietnam COVID-19 vaccine cost?» (en anglès). Voice of Vietnam, 11-12-2020.
- ↑ Hanh, Thuy. «Local Nanocovax vaccine's phase 3 trial to begin next week» (en anglès). Vietnamnet.vn, 26-05-2021. [Consulta: 28 maig 2021].
- ↑ Nguyen, Thuy (Nanogen Pharmaceutical Biotechnology Joint Stock Company). «Study to Evaluate the Safety, Immunogenicity, and Efficacy of Nanocovax Vaccine Against COVID-19» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 11 juny 2021; IDNCT04922788. [Consulta: 11 juny 2021].
- ↑ Le C, Thu A «Vietnam enters second phase of Covid-19 vaccine trials» (en anglès). VnExpress, 26-02-2021.
- ↑ Onishi, Tomoya. «Vietnam homegrown COVID vaccine heads for full approval by year-end» (en anglès). Nikkei Asia, 15-06-2021.
- ↑ Wang, Chang-Yi (United Biomedical Inc.). «A Study to Evaluate UB-612 COVID-19 Vaccine in Adolescent, Younger and Elderly Adult Volunteers» (en anglès). ClinicalTrials.gov, 26 febrer 2021; IDNCT04773067. [Consulta: 20 març 2021].
- ↑ Heppner, Gray (Vaxxinity, Inc.). «A Study to Evaluate the Safety, Immunogenicity, and Efficacy of UB-612 COVID-19 Vaccine» (en anglès). ClinicalTrials.gov, 24 desembre 2020; IDNCT04683224. [Consulta: 20 març 2021].
- ↑ Liao, George «Taiwan's second domestic COVID vaccine's midterm performance in phase II trials inferior to local competitor: experts» (en anglès). Taiwan News, 27-06-2021 [Consulta: 8 juliol 2021].
- ↑ Wang, Chang-Yi (United Biomedical Inc., Asia). «A Study to Evaluate the Safety, Tolerability, and Immunogenicity of UB-612 COVID-19 Vaccine» (en anglès). Clinicaltrials.gov, US National Library of Medicine, 11 setembre 2020; IDNCT04545749. [Consulta: 20 març 2021].
- ↑ Strong, Matthew «Taiwan’s United Biomedical applies for COVID vaccine EUA» (en anglès). Taiwan News, 30-06-2021.
- ↑ Clover Biopharmaceuticals AUS Pty Ltd. «SCB-2019 as COVID-19 Vaccine» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 28 maig 2020; IDNCT04405908. [Consulta: 14 juliol 2020].
- ↑ «Clover Biopharmaceuticals starts Phase I Covid-19 vaccine trial». Clinical Trials Arena, 20-06-2020. Arxivat de l'original el 11 octubre 2020.
- ↑ «About Us». Arxivat de l'original el 11 octubre 2020.
- ↑ Clover Biopharmaceuticals AUS Pty Ltd. «A Controlled Phase 2/3 Study of Adjuvanted Recombinant SARS-CoV-2 Trimeric S-protein Vaccine (SCB-2019) for the Prevention of COVID-19 (SCB-2019)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 17 desembre 2020; IDNCT04672395. [Consulta: 10 març 2021].
- ↑ «Clover Biopharmaceuticals and Dynavax Announce First Participants Dosed in SPECTRA, a Global Phase 2/3 Clinical Trial for Adjuvanted S-Trimer COVID-19 Vaccine Candidate». Dynavax, 24-03-2021.
- ↑ Li, Shawn (Zhejiang Clover Biopharmaceuticals, Inc.). «Immunogenicity and Safety Study of Adjuvanted SARS-CoV-2 (SCB-2019) Vaccine in Adults in China» (en anglès). ClinicalTrials.gov, 8 juliol 2021; IDNCT04954131. [Consulta: 8 juliol 2021].
- ↑ «A Phase 2/3 Study of S-268019». Japan Registry of Clinical Trials.
- ↑ «A Phase 3 Study of S-268019 for the Prevention of COVID-19», 28-01-2022.
- ↑ «Safety and Immunogenicity of an Intranasal RSV Vaccine Expressing SARS-CoV-2 Spike Protein (COVID-19 Vaccine) in Adults». Japan Registry of Clinical Trials.
- ↑ WestVac Biopharma Co. Ltd. «A Global Phase III Clinical Trial of Recombinant COVID-19 Vaccine (Sf9 Cells)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 27 maig 2021; IDNCT04904471. [Consulta: 15 agost 2021].
- ↑ Zhu, Fengcai (Jiangsu Province Centers for Disease Control and Prevention). «Phase I Trial of a Recombinant SARS-CoV-2 Vaccine (Sf9 Cell)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 28 agost 2020; IDNCT04530656. [Consulta: 20 març 2021].
- ↑ Zhu, Fengcai (Jiangsu Province Centers for Disease Control and Prevention). «A Phase II Clinical Trial of Recombinant Corona Virus Disease-19 (COVID-19) Vaccine (Sf9 Cells)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 23 novembre 2020; IDNCT04640402. [Consulta: 20 març 2021].
- ↑ Zhu, Fengcai (Jiangsu Provincial Center for Diseases Control and Prevention). «Phase IIb Clinical Trial of Recombinant Novel Coronavirus Pneumonia (COVID-19) Vaccine (Sf9 Cells)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 22 gener 2021; IDNCT04718467. [Consulta: 20 març 2021].
- ↑ «A Phase III Clinical Trial of Influenza Virus Vector COVID- 19 Vaccine for Intranasal Spray (DelNS1-2019-nCoV-RBD-OPT1)». Chinese Clinical Trial Registry.
- ↑ «A Phase I Clinical Trial of Influenza virus Vector COVID-19 Vaccine for intranasal Spray (DelNS1-2019-nCoV-RBD-OPT1)». Chinese Clinical Trial Registry.
- ↑ «A Phase II Clinical Trial of Influenza virus Vector COVID-19 Vaccine for intranasal Spray (DelNS1-2019-nCoV-RBD-OPT1)». Chinese Clinical Trial Registry.
- ↑ Alves, Vinícius; Figueiredo, Thaisa «Entenda ponto a ponto a Versamune, vacina contra a Covid-19 financiada pelo governo federal» (en portuguès). G1 Globo Notícias, 26-03-2021 [Consulta: 19 setembre 2021].
- ↑ 150,0 150,1 Alvim, Mariana «Vacina Versamune: o que se sabe sobre imunizante anunciado pelo governo federal» (en portuguès). BBC News Brazil, 26-03-2021 [Consulta: 19 setembre 2021].
- ↑ Hospital do Coracao. «Randomized Controlled-trial to Evaluate Safety and Immunogenicity of a Novel Vaccine for Prevention of Covid-19 in Adults Previously Immunized» (en anglès). Clinicaltrials.gov, 23 agost 2021; IDNCT05016934. [Consulta: 23 agost 2021].
- ↑ «A Phase I clinical trial to evaluate the safety, tolerance and preliminary immunogenicity of different doses of a SARS-CoV-2 mRNA vaccine in population aged 18–59 years and 60 years and above», 24-06-2020. Arxivat de l'original el 11 octubre 2020.
- ↑ «Company introduction». Arxivat de l'original el 11 octubre 2020.
- ↑ «A Phase III Clinical Study to Evaluate the Protective Efficacy, Safety, and Immunogenicity of a SARS-CoV-2 Messenger Ribonucleic Acid (mRNA) Vaccine Candidate in Population Aged 18 Years and Above». Chinese Clinical Trial Registry.
- ↑ «A Phase II clinical trial to evaluate the immunogenicity and safety of different doses of a novel coronavirus pneumonia (COVID-19) mRNA vaccine in population aged 18-59 years». Chinese Clinical Trial Registry.
- ↑ «Recombinant SARS-CoV-2 Fusion Protein Vaccine (V-01) Phase III (COVID-19)», 27-10-2021.
- ↑ «评价重组新型冠状病毒融合蛋白疫苗在健康人群免疫原性和安全性随机、双盲、安慰剂对照的II期临床试验». Chinese Clinical Trial Registry.
- ↑ «评价重组新型冠状病毒融合蛋白疫苗在健康人群安全性和免疫原性随机、双盲、安慰剂对照的I期临床试验». Chinese Clinical Trial Registry.
- ↑ «Arcturus Therapeutics Collaborates with Vingroup to Establish Manufacturing Facility in Vietnam for Arcturus’ Investigational mRNA Vaccines for COVID-19». Business Wire, 02-08-2021.
- ↑ Giang, Nguyen Kieu. «Arcturus Allows Vietnam’s Vingroup to Make Covid Vaccines» (en anglès). Bloomberg News, 02-08-2021.
- ↑ «Vingroup collaborates with Arcturus Therapeutics to establish a manufacturing facility in Vietnam for Arcturus’ mRNA Covid-19 vaccine» (en anglès). 'Yahoo! Finance', 02-08-2021.
- ↑ «Arcturus to start clinical trial of COVID-19 vaccine in Vietnam». Reuters, 02-08-2021.
- ↑ «Arcturus Therapeutics lines up Phase 1/2/3 trial for next-generation mRNA COVID-19 vaccine». Biopharma Reporter, 02-08-2021.
- ↑ Vinbiocare Biotechnology Joint Stock Company. «The ARCT-154 Self-Amplifying RNA Vaccine Efficacy Study (ARCT-154-01) (ARCT-154-01)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 19 agost 2021; IDNCT05012943. [Consulta: 19 agost 2021].
- ↑ «Efficacy, Safety, and Immunogenicity Study of the Recombinant Two-component COVID-19 Vaccine (CHO Cell) (ReCOV)», 20-10-2021.
- ↑ «Safety, Reactogenicity and Immunogenicity Study of ReCOV», 26-03-2021.
- ↑ «A Phase I/II Randomized, Multi-Center, Placebo-Controlled, Dose-Escalation Study to Evaluate the Safety, Immunogenicity and Potential Efficacy of an rVSV-SARS-CoV-2-S Vaccine (IIBR-100) in Adults», 01-11-2020.
- ↑ «Phase 2b Dose-confirmatory Trial to Evaluate the Safety, Immunogenicity and Potential Efficacy of an VSV-ΔG SARS-CoV-2 Vaccine (BRILIFE001)», 29-07-2021.
- ↑ Jeffay, Nathan. «As Israel goes vaccine-wild, will the homegrown version lose its shot?» (en anglès). The Times of Israel, 29-12-2020. [Consulta: 1r gener 2021].
- ↑ «Efficacy, safety and immunogenicity of a recombinant protein subunit vaccine (CHO cells) against COVID-19 in adults: an international multicenter, randomized, double-blind, placebo-controlled phase III study». Chinese Clinical Trial Registry, 05-09-2021.
- ↑ «Phase I Trial of a Recombinant COVID-19 Vaccine (CHO Cell)». United States National Library of Medicine, 19-11-2020.
- ↑ Zhu, Fengcai (Jiangsu Province Centers for Disease Control and Prevention). «Immunogenicity and Safety of Recombinant COVID-19 Vaccine (CHO Cells)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 24 març 2021; IDNCT04813562. [Consulta: 13 abril 2021].
- ↑ «Safety and Immunogenicity Study of GX-19, a COVID-19 Preventive DNA Vaccine in Healthy Adults», 24-06-2020. Arxivat de l'original el 11 octubre 2020.
- ↑ Woo, JungWon; Choi, Jun Yong (Genexine, Inc./Severance Hospital). «Safety and Immunogenicity Study of GX-19N, a COVID-19 Preventive DNA Vaccine in Healthy Adults Safety and Immunogenicity» (en anglès). ClinicalTrials.gov, US National Library of Medicine, 20 gener 2021; IDNCT04715997. [Consulta: 16 març 2021].
- ↑ «S. Korea's Genexine begins human trial of coronavirus vaccine». Reuters, 19-06-2020.
- ↑ International Vaccine Institute «Genexine consortium's Covid-19 vaccine acquires approval for clinical trails in Korea» (en anglès). News and stories, 11-06-2020 [Consulta: 1r agost 2020].
- ↑ Choi, Jun Yong (Genexine, Inc.). «Safety and Immunogenicity of GX-19N, a COVID-19 Preventive DNA Vaccine in Elderly Individuals» (en anglès). ClinicalTrials.gov, US National Library of Medicine, 7 juny 2021; IDNCT04915989. [Consulta: 8 juny 2021].
- ↑ Woo, JungWon (Genexine, Inc./PT Kalbe Farma TBK). «Evaluation of Efficacy, Safety and Immunogenicity of GX-19N in Healthy Individuals Who Have Received COVID-19 Vaccines» (en anglès). ClinicalTrials.gov; US National Library of Medicine, 5 octubre 2021; IDNCT05067946. [Consulta: 5 octubre 2021].
- ↑ Lanini, Simone (ReiThera Srl). «GRAd-COV2 Vaccine Against COVID-19» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 7 gener 2021; IDNCT04528641.
- ↑ PRNewswire «ReiThera Announces its GRAd-COV2 COVID-19 Vaccine Candidate is Well Tolerated and Induces Clear Immune Responses in Healthy Subjects Aged 18–55 Years» (en anglès). ReiThera Srl. Yahoo! Finance, 24-11-2020 [Consulta: 12 gener 2021].
- ↑ ReiThera Srl. «Study of GRAd-COV2 for the Prevention of COVID-19 in Adults (COVITAR)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 10 març 2021; IDNCT04791423. [Consulta: 20 març 2021].
- ↑ «REITHERA’S COVID-19 VACCINE CANDIDATE ENTERS PHASE 2/3 CLINICAL STUDY». Reithera, 18-03-2021.
- ↑ Agenzia Nazionale Stampa Associata (ANSA). «New ReiThera vaccine safe, response peak at 4 wks» (en anglès). Latest News, 05-01-2021.
- ↑ «Safety, Immunogenicity, and Efficacy of INO-4800 for COVID-19 in Healthy Seronegative Adults at High Risk of SARS-CoV-2 Exposure». United States National Library of Medicine.
- ↑ «Safety, Tolerability and Immunogenicity of INO-4800 Followed by Electroporation in Healthy Volunteers for COVID19». United States National Library of Medincine.
- ↑ «A Phase II, Randomized, Double-Blinded, Placebo-Controlled, Dose-Finding Clinical Trial to Evaluate the Safety and Immunogenicity of Different Doses of COVID-19 DNA Vaccine INO-4800 Administered Intradermally Followed by Electroporation in Healthy Adult and Elderly Volunteers». Chinese Clinical Trial Registry.
- ↑ Daiichi Sankyo. "Daiichi Sankyo Initiates Phase 1/2 Clinical Trial for mRNA COVID-19 vaccine in Japan". Nota de premsa.
- ↑ «Daiichi takes mRNA COVID-19 vaccine into clinic as Japanese R&D belatedly fires up». Fierce Biotech, 22-03-2021.
- ↑ «既承認SARS-CoV-2 ワクチンの初回接種完了者を対象としたDS-5670a による追加免疫効果を検討する第I/II/III 相、無作為化、実薬対照、評価者盲検試験», 28-12-2021.
- ↑ «Study of DS-5670a (COVID-19 Vaccine) in Japanese Healthy Adults and Elderly Subjects», 29-03-2021.
- ↑ SK Bioscience «SK Bioscience Submitted Phase 3 IND for COVID-19 Vaccine» (en anglès). News Room, 28-06-2021 [Consulta: 28 agost 2021].
- ↑ Cheong, Hee Jin (SK Bioscience Co., Ltd.). «A Phase III Study to Assess the Immunogenicity and Safety of SK SARS-CoV-2 Recombinant Nanoparticle Vaccine Adjuvanted With AS03 (GBP510) in Adults Aged 18 Years and Older» (en anglès). ClinicalTrials.gov, 17 agost 2021; IDNCT05007951. [Consulta: 17 agost 2021].
- ↑ Cheong, Hee Jin (SK Bioscience Co., Ltd). «Safety and Immunogenicity Study of SARS-CoV-2 Nanoparticle Vaccine (GBP510) Adjuvanted With or Without AS03 (COVID-19)» (en anglès). ClinicalTrials.gov, 11 febrer 2021; IDNCT04750343. [Consulta: 22 abril 2021].
- ↑ Cheong, Hee Jin (SK Bioscience Co., Ltd). «Safety and Immunogenicity Study of SARS-CoV-2 Nanoparticle Vaccine (GBP510) Adjuvanted With Aluminum Hydroxide (COVID-19)» (en anglès). ClinicalTrials.gov, 8 febrer 2021; IDNCT04742738. [Consulta: 22 abril 2021].
- ↑ Ministry of Science & Technology, India «Indigenous mRNA vaccine candidate supported by DBT gets Drug Controller nod to initiate Human clinical trials» (en anglès). Press Information Bureau, 11-12-2020 [Consulta: 13 gener 2021].
- ↑ «mRNA Vaccines – HGC019».
- ↑ «Safety and immunogenicity study of an mRNA based vaccine (HGCO19) for COVID19 in healthy adult participants.». Clinical Trials Registry India.
- ↑ «Pune-based Gennova to begin human trials of its Covid vaccine 'soon'». The Indian Express, 15-12-2020.
- ↑ «Safety and immunogenicity study of mRNA based vaccine (HGCO19) against COVID-19 in healthy adult participants.». Clinical Trials Registry India.
- ↑ «Safety and immunogenicity study of mRNA based vaccine (HGCO19) against COVID-19 in healthy adult participants». Cochrane COVID-19 Study Register, 04-08-2021. Arxivat de l'original el 2021-09-11.
- ↑ {Cite web|title=18歳以上の健康な日本人を対象に、COVID-19に対するワクチン(KD-414)を2回接種した際の免疫原性及び安全性を確認する多施設共同非盲検非対照試験。 |url=https://jrct.niph.go.jp/latest-detail/jRCT2071210081 |website=jrct.niph.go.jp |publisher=Japan Registry of Clinical Trials |access-date= 22 octubre 2021 }}
- ↑ «Japan's KM Biologics begins clinical trial of COVID-19 vaccine candidate». Reuters, 22-03-2021.
- ↑ «20歳以上65歳未満の健康成人、及び65歳以上の健康な高齢者を対象に、COVID-19に対するワクチン(KD-414)の安全性及び免疫原性を検討するための、プラセボを対照とする多施設共同二重盲検ランダム化並行群間比較試験». Japan Registry of Clinical Trials.
- ↑ «Immunogenicity and safety of a SARS-CoV-2 Vaccine LYB001 against COVID-19 in healthy adults: a randomized, double blinded, placebo-controlled phase II trial and a single-armed, open-label expanded safety phase III trial». Chinese Clinical Trial Registry.
- ↑ «Safety, Reactogenicity, and Immunogenicity of a Recombinant SARS-CoV-2 Vaccine LYB001 in healthy adults: a randomized, double blinded, placebo-controlled phase I trial.». Chinese Clinical Trial Registry.
- ↑ «A study to assess the safety and immunogenicity of Anti-COVID-19 AKS-452 vaccine for SARS-Сov-2 infection in Indian healthy subjects.», 11-10-2021.
- ↑ «Anti-COVID19 AKS-452 – ACT Study (ACT)», 23-12-2020.
- ↑ AnGes, Inc. Clinical Development. «Study of COVID-19 DNA Vaccine (AG0302-COVID19)» (en anglès). Cclinicaltrials.gov, United States National Library of Medicine, 26 agost 2020; IDNCT04527081. [Consulta: 11 març 2021].
- ↑ «About AnGes – Introduction». Arxivat de l'original el 11 octubre 2020.
- ↑ AnGes, Inc. Clinical Development. «Phase II / III Study of COVID-19 DNA Vaccine (AG0302-COVID19)» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 7 desembre 2020; IDNCT04655625. [Consulta: 11 març 2021].
- ↑ «Phase II Clinical Trial of Recombinant SARS-CoV-2 Spike Protein Vaccine (CHO Cell)», 04-08-2021.
- ↑ «Phase I Clinical Trial of Recombinant SARS-CoV-2 Spike Protein Vaccine (CHO Cell)», 04-07-2021.
- ↑ «A Ph 2 Trial With an Oral Tableted COVID-19 Vaccine», 05-10-2021.
- ↑ «Safety and Immunogenicity Trial of an Oral SARS-CoV-2 Vaccine (VXA-CoV2-1) for Prevention of COVID-19 in Healthy Adults», 24-09-2020.
- ↑ «Ph 1b: Safety & Immunogenicity of Ad5 Based Oral Norovirus Vaccine (VXA-NVV-104)», 22-04-2021.
- ↑ 216,0 216,1 «Made-in-Canada coronavirus vaccine starts human clinical trials». Canadian Broadcasting Corporation, 26-01-2021.
- ↑ «PTX-COVID19-B, an mRNA Humoral Vaccine, Intended for Prevention of COVID-19 in a General Population. This Study is Designed to Demonstrate the Safety, Tolerability, and Immunogenicity of PTX-COVID19-B in Comparison to the Pfizer-BioNTech COVID-19 Vaccine.», 04-01-2022.
- ↑ «PTX-COVID19-B, an mRNA Humoral Vaccine, is Intended for Prevention of COVID-19 in a General Population. This Study is Designed to Evaluate Safety, Tolerability, and Immunogenicity of PTX-COVID19-B Vaccine in Healthy Seronegative Adults Aged 18-64», 21-02-2021.
- ↑ «Randomized, double-blind, placebo-controlled phase II clinical trial of immunogenicity, immunopersistence, and safety of graded Novel Coronavirus inactivated vaccine (Vero cells) in healthy persons aged 18 years and older», 29-09-2021.
- ↑ «A randomized, double-blind, placebo-controlled phase I clinical trial to evaluate the safety and immunogenicity of the Novel Coronavirus inactivated vaccine (Vero cells) in healthy individuals 18 years of age and older», 16-08-2021.
- ↑ «Another Chinese adenovirus vector COVID-19 vaccine ready for human trials». Xinhua, 28-12-2020.
- ↑ Zhu, Fengcai (Jiangsu Province Centers of Disease Control and Prevention). «A Phase II Clinical Trial to Evaluate the Recombinant Vaccine for COVID-19 (Adenovirus Vector) (CTII-nCoV)» (en anglès). ClinicalTrials.gov, US National Library of Medicine, 10 abril 2021; IDNCT04341389. [Consulta: 3 desembre 2021].
- ↑ «Phase I Clinical Trial of the Candidate Recombinant SARS-CoV-2 Vaccine (Chimpanzee Adenoviral Vector)», 23-05-2021.
- ↑ «INNA-051 intranasal safety and tolerability study», 12-11-2021.
- ↑ «INNA-051 intranasal safety and tolerability study», 21-04-2021.
- ↑ «A Study to Evaluate the Immunogenicity and Safety of mRNA-1283 COVID-19 Vaccine Boosters», 30-11-2021.
- ↑ «A Study to Evaluate Safety, Reactogenicity, and Immunogenicity of mRNA-1283 and mRNA-1273 Vaccines in Healthy Adults Between 18 Years and 55 Years of Age to Prevent COVID-19», 24-03-2021.
- ↑ Gursel, I. «Study of a Severe Acute Respiratory Syndrome Coronavirus-2 (SARS-CoV-2) Virus-like Particle (VLP) Vaccine (COVID-19)» (en anglès). ClinicalTrials.gov, 15 juliol 2021; IDNCT04962893. [Consulta: 15 juliol 2021].
- ↑ Gursel, I; Yurtaslan, A. «Study of a Severe Acute Respiratory Syndrome CoV-2 (SARS-CoV-2) Virus-like Particle (VLP) Vaccine in Healthy Adults (COVID-19)» (en anglès). ClinicalTrials.gov, 13 juliol 2021 (rev); IDNCT04818281. [Consulta: 17 juliol 2021].
- ↑ Dadwal, Sanjeet S. (City of Hope Medical Center). «SARS-CoV-2 Vaccine (COH04S1) Versus Emergency Use Authorization SARS-COV-2 Vaccine for the Treatment of COVID-19 in Patients With Blood Cancer» (en anglès). ClinicalTrials.gov, 26 juliol 2021; IDNCT04977024. [Consulta: 28 juliol 2021].
- ↑ Zaia, John (City of Hope Medical Center). «A Synthetic MVA-based SARS-CoV-2 Vaccine, COH04S1, for the Prevention of COVID-19» (en anglès). ClinicalTrials.gov, 20 novembre 2021; NCT04639466. [Consulta: 26 juliol 2021].
- ↑ «Bavarian Nordic reports encouraging preclinical data for COVID-19 vaccine candidate ahead of first-in-human trial». , 08-03-2021.
- ↑ Bavarian Nordic «Bavarian Nordic Initiates Phase 2 Clinical Trial of COVID-19 Booster Vaccine» (en anglès). Company Announcement 26/2021, 23-08-2021 [Consulta: 24 agost 2021].
- ↑ Bavarian Nordic. «ABNCoV2 Vaccine in SARS-CoV-2 Seronegative and Seropositive Adult Subjects» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 14 octubre 2021; IDNCT05077267. [Consulta: 14 octubre 2021].
- ↑ Radboud University. «Safety and Tolerability of ABNCoV2 (COUGH-1)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 9 abril 2021; IDNCT04839146. [Consulta: 13 abril 2021].
- ↑ Limon, Raul «First Spanish Covid-19 vaccine approved for human clinical trial». El Pais, 12-08-2021 [Consulta: 15 agost 2021].
- ↑ «Safety and Immunogenicity Study of Recombinant Protein RBD Candidate Vaccine Against SARS-CoV-2 in Adult Healthy Volunteers (COVID-19)», 16-08-2021.
- ↑ «Safety and Immunogenicity of Recombinant Protein RBD Fusion Dimer Vaccine Against the Virus That Cause COVID-19, Known as Severe Acute Respiratoy Syndrome Coronavirus 2 (SARS-CoV-2)», 02-12-2021.
- ↑ «COVID-19». CureVac.
- ↑ CureVac AG/BMBF. «COVID-19: A Phase2b/3, Randomized, Observer-Blinded, Placebo Controlled, Multicenter Clinical Study Evaluating the Efficacy and Safety of Investigational SARS-CoV-2 mRNA Vaccine CVnCoV in Adults 18 Years of Age and Older» (en anglès). EU Clinical Trials Register, 19 desembre 2020; ID2020-003998-22.
- ↑ CureVac AG/German Federal Ministry of Education and Research. «A Study to Evaluate the Safety and Immunogenicity of Vaccine CVnCoV in Healthy Adults in Germany for COVID-19» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 19 desembre 2020; IDNCT04674189. [Consulta: 23 març 2021].
- ↑ CureVac AG. «A Study to Evaluate the Immunogenicity and Safety of the SARS-CoV-2 mRNA Vaccine CVnCoV in Elderly Adults Compared to Younger Adults for COVID-19» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 9 abril 2020; IDNCT04838847. [Consulta: 26 abril 2021].
- ↑ CureVac AG. «A Study to Evaluate Safety, Reactogenicity and Immunogenicity of the SARS-CoV-2 mRNA Vaccine CVnCoV in Adults With Co-morbidities for COVID-19» (en anglès). Clinicaltrials.gov, United States National Library of Medicine, 26 abril 2021; IDNCT04860258. [Consulta: 26 abril 2021].
- ↑ «COVID-19: A Phase 2b/3, Randomized, Observer-Blinded, Placebo Controlled, Multicenter Clinical Study Evaluating the Efficacy and Safety of Investigational SARS-CoV-2 mRNA Vaccine CVnCoV in Adults 18 Years of Age and Older», 19-11-2020.
- ↑ «A Study to Evaluate the Safety, Reactogenicity and Immunogenicity of Vaccine CVnCoV in Healthy Adults», 26-06-2020. Arxivat de l'original el 11 octubre 2020.
- ↑ «A Dose-Confirmation Study to Evaluate the Safety, Reactogenicity and Immunogenicity of Vaccine CVnCoV in Healthy Adults», 17-08-2020. Arxivat de l'original el 23 agost 2020.
- ↑ Keystone-SDA/Reuters/sb. «CureVac seeks Covid-19 shot approval in Switzerland» (en angles). Science, SWI swissinfo.ch, 20-04-2021. [Consulta: 17 març 2021].
- ↑ Ledford, Heidi «Could mixing COVID vaccines boost immune response?» (en anglès). Nature, 590, 7846, 18-02-2021, pp: 375–376. DOI: 10.1038/d41586-021-00315-5. ISSN: 0028-0836.
- ↑ Al Jazeera «Angela Merkel receives Moderna dose after first AstraZeneca shot» (en anglès). News, 22-06-2021 [Consulta: 28 juny 2021].
- ↑ Stuart, Arabella; Shaw, Robert; Walker, Laura «Comparing coronavirus (COVID-19) vaccine schedule combinations» (en anglès). ISRCTN Registry, 29-01-2021. DOI: 10.1186/ISRCTN69254139. ISRCTN69254139 [Consulta: 9 juliol 2021].
- ↑ Russian Direct Investment Fund «Combination of the first component of Sputnik V vaccine (Sputnik Light vaccine) with vaccines by AstraZeneca, Sinopharm and Moderna demonstrates high safety profile during the study in Argentina's Buenos-Aires province» (en anglès). Press Releases [Moscow], 04-08-2021 [Consulta: 5 agost 2021]. «Còpia arxivada». Arxivat de l'original el 2021-08-05. [Consulta: 6 agost 2021].
- ↑ Vichos, Iason; Snape, Matthew «Comparing COVID-19 vaccine schedule combinations – stage 2» (en anglès). ISRCTN Registry, 12-03-2021. DOI: 10.1186/ISRCTN27841311. ISRCTN27841311 [Consulta: 9 juliol 2021].
- ↑ Li, Jing-Xin (Jiangsu Provincial Center for Diseases Control and Prevention) «Study on Sequential Immunization of Recombinant COVID-19 Vaccine (Ad5 Vector) and RBD-based Protein Subunit Vaccine» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 6 abril 2021; IDNCT04833101 [Consulta: 9 juliol 2021].
- ↑ Frías Iniesta, Jesus (Spanish Clinical Research Network - SCReN) «Vaccination With COMIRNATY in Subjects With a VAXZEVRIA First Dose (CombiVacS)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 27 abril 2021; IDNCT04860739 [Consulta: 9 juliol 2021].
- ↑ Langley, Joanne (Canadian Immunization Research Network) «Mix and Match of the Second COVID-19 Vaccine Dose for Safety and Immunogenicity (MOSAIC)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 20 maig 2021; IDNCT04894435 [Consulta: 9 juliol 2021].
- ↑ Launay, Odile; Janssen, Cécile (Assistance Publique - Hôpitaux de Paris) «Compare Immunological Efficacy of a Vaccine Regimen Combining Two Covid19 mRNA Vaccines (Pfizer-BioNTech and Moderna) With That of a Homologous Vaccination of Each Covid19 mRNA Vaccine (ARNCOMBI)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 25 maig 2021; IDNCT04900467 [Consulta: 9 juliol 2021].
- ↑ von Laer, Dorothee; Kimpel, Janine (Medical University Innsbruck) «Heterologous Vaccination With an Vaxzevria (ChAdOx1-S) Prime and a Comirnaty (BNT162b2) Boost Compared With Homolog Vaccination With Vaxzervria (Prime/Boost) or Comirnaty (Prime/Boost) (HeVacc)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 28 maig 2021; IDNCT04907331 [Consulta: 9 juliol 2021].
- ↑ van der Kuy, Hugo (Erasmus Medical Center) «A Trial Among HealthCare Workers (HCW) Vaccinated With Janssen Vaccine: the SWITCH Trial (SWITCH)» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 16 juny 2021; IDNCT04927936 [Consulta: 9 juliol 2021].
- ↑ Branswell, Helen. «Comparing three Covid-19 vaccines: Pfizer, Moderna, J&J» (en anglès). Stat, 02-02-2021. [Consulta: 28 febrer 2021].
- ↑ Prieto-Alhambra, D «The comparative effectiveness of the different COVID vaccines: where do we stand?» (en anglès). Enf Emerg, 2021; 20 (1), pp: 4-6. ISSN: 2013-844X [Consulta: 31 desembre 2021].
- ↑ Randolph HE, Barreiro LB «Herd Immunity: Understanding COVID-19» (en anglès). Immunity, 52, 5, 19-05-2020, pp: 737–741. DOI: 10.1016/j.immuni.2020.04.012. PMC: 7236739. PMID: 32433946.
- ↑ Stenson, Jacqueline. «The FDA's cutoff for Covid-19 vaccine effectiveness is 50 percent. What does that mean?» (en anglès). NBC News, 03-11-2020. [Consulta: 8 gener 2021].
- ↑ Oakes, Kari. «EMA sets 50% efficacy goal – with flexibility – for COVID vaccines» (en anglès). Regulatory Affairs Professionals Society, 19-11-2020. [Consulta: 8 gener 2021].
- ↑ Bartsch, Sarah; O'Shea, Kelly; Ferguson, Marie; Bottazzi, Maria; Wedlock, Patrick; Strych, Ulrich; McKinnell, James; Siegmund, Sheryl; et al «Vaccine Efficacy Needed for a COVID-19 Coronavirus Vaccine to Prevent or Stop an Epidemic as the Sole Intervention» (en anglès). American Journal of Preventive Medicine, 59, 4, 15-07-2020, pp: 493–503. DOI: 10.1016/j.amepre.2020.06.011. PMC: 7361120. PMID: 32778354 [Consulta: 6 març 2021].
- ↑ Dean, Natalie; Madewell, Zachary. «Understanding the spectrum of vaccine efficacy measures» (en anglès). The BMJ Opinion, 05-03-2021. [Consulta: 10 març 2021].
- ↑ «Single-dose administration and the influence of the timing of the booster dose on immunogenicity and efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine: a pooled analysis of four randomised trials». Lancet, 397, 10277, 3-2021, pàg. 881–91. DOI: 10.1016/S0140-6736(21)00432-3. PMC: 7894131. PMID: 33617777.
- ↑ AstraZeneca. «AZD1222 US Phase III primary analysis confirms safety and efficacy» (en anglès). Press Releases, Media centre, 25-03-2021. [Consulta: 25 març 2021].
- ↑ 268,0 268,1 DailyMed. «Drug label Information: Pfizer–BioNTech COVID-19 Vaccine – rna ingredient bnt-162b2 injection, suspension» (en anglès). NIH/NLM, US National Institutes of Health, 2 setembre 2021 (rev). [Consulta: 13 setembre 2020].
- ↑ Committee for Medicinal Products for Human Use, European Medicines Agency (EMA) «COVID-19 Case Definitions; tables 2, 5, 12, 13» (en anglès). A: European public report: Comirnaty (COVID-19 mRNA vaccine (nucleoside-modified), 2021 Feb 19; EMA/707383/2020 (rev. 1), pàgs: 58, 80, 90 [Consulta: 23 juny 2021].
- ↑ 270,0 270,1 «Janssen COVID-19 Vaccine - ad26.cov2.s injection, suspension». U.S. National Institutes of Health.
- ↑ «FDA Briefing Document: Janssen Ad26.COV2.S Vaccine for the Prevention of COVID-19». US Food & Drug Administration (FDA), 26-02-2021.
- ↑ DailyMed. «Drug Label Information: Moderna COVID-19 Vaccine- cx-024414 injection, suspension» (en anglès). NIH/NLM, US National Institutes of Health, 8 setembre 2021 (rev). [Consulta: 13 setembre 2021].
- ↑ 273,0 273,1 Al Kaabi N, Zhang Y, Xia S, Yang Y, Al Qahtani MM, Abdulrazzaq N, Al Nusair M, Hassany M, Jawad JS, Abdalla J, Hussein SE, Al Mazrouei SK, Al Karam M, Li X, et al «Effect of 2 Inactivated SARS-CoV-2 Vaccines on Symptomatic COVID-19 Infection in Adults: A Randomized Clinical Trial» (en anglès). JAMA, 2021 Jul 6; 326 (1), pp: 35-45. DOI: 10.1001/jama.2021.8565. PMC: 8156175. PMID: 34037666.
- ↑ Interim recommendations for use of the inactivated COVID-19 vaccine BIBP developed by China National Biotec Group (CNBG), Sinopharm (Guidance). World Health Organization. 7 maig 2021. WHO/2019-nCoV/vaccines/SAGE_recommendation/BIBP/2021.1.
- ↑ «Safety and efficacy of an rAd26 and rAd5 vector-based heterologous prime-boost COVID-19 vaccine: an interim analysis of a randomised controlled phase 3 trial in Russia». The Lancet, 397, 10275, 2-2021, pàg. 671–681. DOI: 10.1016/S0140-6736(21)00234-8. ISSN: 0140-6736. PMC: 7852454. PMID: 33545094.
- ↑ Sinovac Biotech «Summary of Clinical Trial Data of Sinovac’s COVID-19 Vaccine (CoronaVac®)-SINOVAC - Supply Vaccines to Eliminate Human Diseases» (en anglès). Press Releases, 03-04-2021 [Consulta: 12 abril 2021].
- ↑ Palacios, Ricardo; Batista, Ana Paula; Santos Nascimento Albuquerque, Camila; González Patiño, Elizabeth; Santos, Joane do Prado; Reis Pessoa Conde, Mônica Tilli; de Oliveira Piorelli, Roberta; Pereira Júnior, Luiz Carlos; Raboni, Sonia Mara; et al «Efficacy and Safety of a COVID-19 Inactivated Vaccine in Healthcare Professionals in Brazil: The PROFISCOV Study» (en anglès). SSRN eLibrary, 14-04-2021. DOI: 10.2139/ssrn.3822780. ISSN: 1556-5068 [Consulta: 7 juliol 2021].
- ↑ 278,0 278,1 Toscano, C; Araos, R; Martí, M. «Evidence Assessment: Sinovac/CoronaVac COVID-19 vaccine» (en anglès). SAGE Working Group on COVID-19 vaccines, WHO, 29-04-2021.
- ↑ Ocugen Inc. «Ocugen's COVID-19 Vaccine Co-Development Partner, Bharat Biotech, Shares Phase 3 Results Demonstrating 77.8% Protection against Overall Disease» (en anglès). COVID-19 News Release, GlobeNewswire [Malvern, Pennsylvania; Hyderabad, India], 02-07-2021 [Consulta: 3 juliol 2021].
- ↑ Russian Direct Investment Fund (6 maig 2021). "Single dose vaccine, Sputnik Light, authorized for use in Russia". Nota de premsa. “The single dose Sputnik Light vaccine demonstrated 79.4% efficacy according to analyzed data taken from 28 days after the injection was administered as part of Russia's mass vaccination program between 5 December 2020 and 15 April 2021.”
- ↑ «CanSinoBIO's COVID-19 vaccine 65.7% effective in global trials, Pakistan official says». Reuters [Islamabad], 08-02-2021. «its single-dose regimen and normal refrigerator storage requirement could make it a favourable option for many countries»
- ↑ BioCubaFarma «Candidato vacunal Abdala muestra 92,28% de eficacia en su esquema único de tres dosis» (en castellà). Noticias Red CVSP, 21-06-2021 [Consulta: 1r juliol 2021].
- ↑ Caraballosa, Eric. «How was the efficacy of the Cuban COVID-19 vaccine candidates calculated?» (en anglès). OnCubaNews English, 27-06-2021. [Consulta: 28 juny 2021].
- ↑ EFE, La Habana «La potencial vacuna cubana Soberana 02 muestra una eficacia del 62% en ensayos» (en castellà). Sociedad: Coronavirus Cuba, 20-06-2021 [Consulta: 1r juliol 2021].
- ↑ Wadman M, Cohen J «Novavax vaccine delivers 89% efficacy against COVID-19 in UK – but is less potent in South Africa» (en anglès). Science ISSN 1095-9203, 28-01-2021.
- ↑ Novavax Inc. «Novavax COVID-19 Vaccine Demonstrates 89.3% Efficacy in UK Phase 3 Trial» (en anglès). Press Releases & Statements, 28-01-2021 [Consulta: 3 març 2021].
- ↑ (14 juny 2021). "Novavax COVID-19 Vaccine Demonstrates 90% Overall Efficacy and 100% Protection Against Moderate and Severe Disease in PREVENT-19 Phase 3 Trial". Nota de premsa.
- ↑ (16 juny 2021). "CureVac Provides Update on Phase 2b/3 Trial of First-Generation COVID-19 Vaccine Candidate, CVnCoV". Nota de premsa.
- ↑ (1 juliol 2021). "Zydus applies to the DCGI for EUA to launch ZyCoV-D, the world's first Plasmid DNA vaccine for COVID-19". Nota de premsa.
- ↑ «China's Zhifei says unit's COVID shot shows 81.76% efficacy in late-stage trial». Reuters, 27-08-2021.
- ↑ (22 setembre 2021). "Clover’s COVID-19 Vaccine Candidate Demonstrates 79% Efficacy Against Delta in Global Phase 2/3 SPECTRA Trial Dominated by Variants of Concern and Interest". Nota de premsa.
- ↑ 292,0 292,1 Office of the Commissioner. «Coronavirus (COVID-19) Update: FDA Issues Policies to Guide Medical Product Developers Addressing Virus Variants» (en anglès). FDA, 23-02-2021. [Consulta: 7 març 2021].
- ↑ Mahase, E «Covid-19: Where are we on vaccines and variants?» (en anglès). News Analysis, BMJ, 372, 02-03-2021, pp: n597. DOI: 10.1136/bmj.n597. ISSN: 1756-1833. PMID: 33653708.
- ↑ 294,0 294,1 294,2 294,3 World Health Organization «COVID-19 Weekly Epidemiological Update. Edition 43, 8 Jun 2021» (en anglès). Situation Report, 08-06-2021 [Consulta: 14 juny 2021].
- ↑ Corum, J; Zimmer, C «Inside the B.1.1.7 Coronavirus Variant» (en anglès). The New York Times, 18-01-2021 [Consulta: 29 gener 2021].
- ↑ Muik A, Wallisch AK, Sänger B, Swanson KA, Mühl J, Chen W, Cai H, Maurus D, Sarkar R, Türeci Ö, Dormitzer PR, Şahin, U «Neutralization of SARS-CoV-2 lineage B.1.1.7 pseudovirus by BNT162b2 vaccine-elicited human sera» (en anglès). Science, 371, 6534, 12-03-2021, pp: 1152–1153. DOI: 10.1126/science.abg6105. PMC: 7971771. PMID: 33514629 [Consulta: 28 setembre 2021].
- ↑ 297,0 297,1 Wang P, Nair MS, Liu L, Iketani S, et al «Antibody Resistance of SARS-CoV-2 Variants B.1.351 and B.1.1.7» (en anglès). Nature, 2021 Maig; 593 (7857), pp: 130-135. DOI: 10.1038/s41586-021-03398-2. ISSN: 1476-4687. PMID: 33684923 [Consulta: 13 agost 2021].
- ↑ Emary KR, Golubchik T, Aley PK, Ariani CV, Angus B, Bibi S, Blane B, Bonsall D, Cicconi P, Charlton S, et al «Efficacy of ChAdOx1 nCoV-19 (AZD1222) vaccine against SARS-CoV-2 variant of concern 202012/01 (B.1.1.7): an exploratory analysis of a randomised controlled trial» (en anglès). Lancet, 2021 Abr 10; 397 (10282), pp: 1351-1362. DOI: 10.1016/S0140-6736(21)00628-0. PMC: 8009612. PMID: 33798499 [Consulta: 13 agost 2021].
- ↑ Mahase, E «Covid-19: Novavax vaccine efficacy is 86% against UK variant and 60% against South African variant» (en anglès). BMJ, 372, 01-02-2021, pp: n296. DOI: 10.1136/bmj.n296. ISSN: 1756-1833. PMID: 33526412.
- ↑ Ray, Siladitya. «Moderna Launches Trial For Covid-19 Vaccine Booster To Tackle South African Strain» (en anglès). Forbes Breaking News, 25-01-2021. [Consulta: 30 gener 2021].
- ↑ Liu Y, Liu J, Xia H, Zhang X, Fontes-Garfias CR, Swanson KA, et al «Neutralizing Activity of BNT162b2-Elicited Serum» (en anglès). The New England Journal of Medicine, 2021 Mar 8; 384 (15), pp: 1466-1468. DOI: 10.1056/nejmc2102017. PMC: 7944950. PMID: 33596352 [Consulta: 28 setembre 2021].
- ↑ 302,0 302,1 Hoffmann M, Arora P, Gross R, Seidel A, Hoernich BF, Hahn AS, Krueger N, Graichen L, Hofmann-Winkler H, et al «SARS-CoV-2 variants B.1.351 and P.1 escape from neutralizing antibodies» (en anglès). Cell, 184, 9, 3-2021, pp: 2384–2393.e12. DOI: 10.1016/j.cell.2021.03.036. PMC: 7980144. PMID: 33794143.
- ↑ Pfizer Inc. «Pfizer and BioNTech Confirm High Efficacy and No Serious Safety Concerns Through Up to Six Months Following Second Dose in Updated Topline Analysis of Landmark COVID-19 Vaccine Study». Press release, 01-04-2021.
- ↑ Johnson & Johnson Services, Inc. «Johnson & Johnson Announces Single-Shot Janssen COVID-19 Vaccine Candidate Met Primary Endpoints in Interim Analysis of its Phase 3 ENSEMBLE Trial» (en anglès). Media Center, 29-01-2021 [Consulta: 29 gener 2021].
- ↑ Francis D, Andy B «Oxford/AstraZeneca COVID shot less effective against South African variant: study» (en anglès). Reuters, 06-02-2021 [Consulta: 8 febrer 2021].
- ↑ 306,0 306,1 Triggle, Nick; Fihlani, Pumza «Covid: South Africa halts AstraZeneca vaccine rollout over new variant» (en anglès). BBC News Online, 08-02-2021 [Consulta: 8 febrer 2021].
- ↑ Booth W, Johnson CY «South Africa suspends Oxford-AstraZeneca vaccine rollout after researchers report 'minimal' protection against coronavirus variant». The Washington Post (Lond), 07-02-2021 [Consulta: 8 febrer 2021]. «South Africa will suspend use of the coronavirus vaccine being developed by Oxford University and AstraZeneca after researchers found it provided 'minimal protection' against mild to moderate coronavirus infections caused by the new variant first detected in that country.»
- ↑ Madhi, Shabir A. (University of Witwatersrand, South Africa); Shinde, Vivek (Novavax, Inc.) «A Phase 2A/B, Randomized, Observer-blinded, Placebo-controlled Study to Evaluate the Efficacy, Immunogenicity, and Safety of a SARS-CoV-2 Recombinant Spike Protein Nanoparticle Vaccine (SARS-CoV-2 rS) With Matrix-M1 Adjuvant in South African Adult Subjects Living Without HIV; and Safety and Immunogenicity in Adults Living With HIV» (en anglès). ClinicalTrials.gov, United States National Library of Medicine, 31-08-2020.
- ↑ «PANGO lineages» (en anglès). cov-lineages.org. Arxivat de l'original el 3 de juny 2021. [Consulta: 18 abril 2021].
- ↑ Koshy, Jacob «Coronavirus | Indian 'double mutant' strain named B.1.617» (en anglès). The Hindu, 08-04-2021.
- ↑ Passifiume, Bryan «India's variant-fuelled second wave coincided with spike in infected flights landing in Canada» (en anglès). Toronto Sun, 10-04-2021 [Consulta: 10 abril 2021].
- ↑ Shrutirupa, Banerjiee. «Is This COVID–20?. Double Mutant Strain Explained» (en anglès). Self Immune, 17-04-2021. [Consulta: 18 abril 2021].
- ↑ 313,0 313,1 Biswas, Soutik «'Double mutant': What are the risks of India's new Covid-19 variant» (en anglès). BBC News Online, 25-03-2021 [Consulta: 11 abril 2021].
- ↑ Haseltine, William A. «An Indian SARS-CoV-2 Variant Lands In California. More Danger Ahead?» (en anglès). Forbes, 12-04-2021 [Consulta: 14 abril 2021].
- ↑ Public Health England «Confirmed cases of COVID-19 variants identified in UK» (en anglès). Gov.UK, News and communications, 15-04-2021 [Consulta: 16 abril 2021].
- ↑ Public Health England. «Expert reaction to VUI-21APR-02/B.1.617.2 being classified by PHE as a variant of concern» (en anglès). Science Media Centre, 07-05-2021. [Consulta: 15 maig 2021].
- ↑ Thorp, H. Holden «Underpromise, overdeliver» (en anglès). Science, 367, 6485, 27-03-2020, pp: 1405. DOI: 10.1126/science.abb8492. ISSN: 1095-9203. PMID: 32205459.
- ↑ «Clinical Development Success Rates 2006–2015». BIO Industry Analysis, 01-06-2016. Arxivat de l'original el 12 setembre 2019. [Consulta: 23 març 2020].
- ↑ 319,0 319,1 Gates, B «Responding to Covid-19: A once-in-a-century pandemic?» (en anglès). The New England Journal of Medicine, 382, 18, 28-02-2020, pp: 1677–1679. DOI: 10.1056/nejmp2003762. ISSN: 1533-4406. PMID: 32109012.
- ↑ Fauci AS, Lane HC, Redfield RR «Covid-19: Navigating the uncharted» (en anglès). The New England Journal of Medicine, 382, 13, 26-03-2020, pp: 1268–1269. DOI: 10.1056/nejme2002387. PMC: 7121221. PMID: 32109011.
- ↑ Mao, Q; Xu, M; He, Q; Li, C, et al «COVID-19 vaccines: progress and understanding on quality control and evaluation» (en anglès). Signal Transduct Target Ther, 2021 Maig 18; 6 (1), pp: 199. DOI: 10.1038/s41392-021-00621-4. PMC: 8129697. PMID: 34006829 [Consulta: 4 novembre 2021].
- ↑ 322,0 322,1 322,2 Iwasaki, Akiko; Yang, Yexin «The potential danger of suboptimal antibody responses in COVID-19» (en anglès). Nature Reviews Immunology, 20, 6, 21-04-2020, pp: 339–341. DOI: 10.1038/s41577-020-0321-6. ISSN: 1474-1733. PMC: 7187142. PMID: 32317716.
- ↑ Wiedermann, Úrsula; Garner-Spitzer, Erika; Wagner, Angelika «Primary vaccine failure to routine vaccines: Why and what to do?» (en anglès). Human Vaccines and Immunotherapeutics, 12, 1, 1-2016, pp: 239–243. DOI: 10.1080/21645515.2015.1093263. ISSN: 2164-554X. PMC: 4962729. PMID: 26836329.
- ↑ Zumla, Alimuddin; Hui, David S.; Perlman, Stanley «Middle East respiratory syndrome» (en anglès). Lancet, 386, 9997, 11-09-2015, pp: 995–1007. DOI: 10.1016/S0140-6736(15)60454-8. PMC: 4721578. PMID: 26049252.
- ↑ Garcia de Jesus, Erin. «Is the coronavirus mutating? Yes. But here's why you don't need to panic» (en anglès). Health & Medicine, Science News, 26-05-2020. [Consulta: 21 juny 2020].
- ↑ Jia, Z; Gong, W «Will Mutations in the Spike Protein of SARS-CoV-2 Lead to the Failure of COVID-19 Vaccines?» (en anglès). J Korean Med Sci, 2021 Maig 10; 36 (18), pp: e124. DOI: 10.3346/jkms.2021.36.e124. PMC: 8111046. PMID: 33975397 [Consulta: 4 novembre 2021].
- ↑ Grove Krause, Tyra. «Mutationer i minkvirus» (en danès). Statens Serum Institut. [Consulta: 6 novembre 2020].
- ↑ AstraZeneca. «Vaxzevria is highly effective after one dose against severe disease or hospitalisation caused by Beta and Delta variants of concern» (en anglès). Media Centre, 23-07-2021. [Consulta: 28 juliol 2021].
- ↑ 329,0 329,1 Dubé, Eve; Laberge, Caroline; Guay, Maryse; Bramadat, Paul; Roy, Réal; Bettinger, Julie «Vaccine hesitancy: an overview» (en anglès). Human Vaccines and Immunotherapeutics, 9, 8, 01-08-2013, pp: 1763–1773. DOI: 10.4161/hv.24657. ISSN: 2164-554X. PMC: 3906279. PMID: 23584253.
- ↑ Howard, Jacqueline; Stracqualursi, Veronica «Fauci warns of 'anti-science bias' being a problem in US» (en anglès). CNN Polítics, 18-06-2020 [Consulta: 21 juny 2020].
- ↑ Winter, SS; Page-Reeves, JM; Page, KA; Haozous, E; Solares, A; Cordova, CN; Larson, RS «Inclusion of special populations in clinical research: important considerations and guidelines» (en anglès). Journal of Clinical and Translational Research, 4, 1, 28-05-2018, pp: 56–69. ISSN: 2382-6533. PMC: 6410628. PMID: 30873495.
- ↑ WHO. «Ten health issues WHO will tackle this year» (en anglès). Newsroom/Spotlight, 2019. [Consulta: 26 maig 2020].
- ↑ Machingaidze, S; Wiysonge, CS «Understanding COVID-19 vaccine hesitancy» (en anglès). Nature Medicine, 2021; Jul 16, pp: 1338-1339. DOI: 10.1038/s41591-021-01459-7. ISSN: 1546-170X. PMID: 34272500 [Consulta: 24 juliol 2021].
- ↑ Malik, Amyn A.; McFadden, SarahAnn M.; Elharake, Jad; Omer, Saad B. «Determinants of COVID-19 vaccine acceptance in the US» (en anglès). EClinicalMedicine, 26, 2020; Set, pp: 100495. DOI: 10.1016/j.eclinm.2020.100495. ISSN: 2589-5370. PMC: 7423333. PMID: 32838242.
- ↑ Thunstrom, L; Madison, A; Finnoff, D; Newbold, S «Hesitancy towards a COVID‑19 vaccine and prospects for herd immunity» (en anglès). SSRN Electronic Journal, 2020; Jun 30. DOI: 10.2139/ssrn.3593098. ISSN: 1556-5068 [Consulta: 7 juliol 2020].[Enllaç no actiu]
- ↑ Beard, David. «Poll shows 61 percent of Americans likely to take COVID-19 vaccine» (en anglès). National Geographic, 03-12-2020. [Consulta: 12 desembre 2020].
- ↑ Xu, S; Huang, R; Sy, LS; Glenn, SC; et al «COVID-19 Vaccination and Non–COVID-19 Mortality Risk - Seven Integrated Health Care Organizations, United States, December 14, 2020–July 31, 2021» (en anglès). MMWR Morb Mortal Wkly Rep, 2021 Oct 29; 70 (43), pp: 1520-1524. DOI: 10.15585/mmwr.mm7043e2. PMC: 8553028. PMID: 34710075 [Consulta: 10 gener 2022].
- ↑ Gates, Bill. «The first modern pandemic: The scientific advances we need to stop COVID-19». The Gates Notes, 23-04-2020. Arxivat de l'original el 13 maig 2020. [Consulta: 6 maig 2020].
- ↑ Sanger, David E.; Kirkpatrick, David D.; Zimmer, Carl; Thomas, Katie; Wee, Sui-Lee «With Pressure Growing, Global Race for a Vaccine Intensifies» (en anglès). The New York Times ISSN 0362-4331, 02-05-2020 [Consulta: 2 maig 2020].
- ↑ Steenhuysen, Julie; Eisler, Peter; Martell, Allison; Nebehay, Stephanie «Special Report: Countries, companies risk billions in race for coronavirus vaccine» (en anglès). Reuters, 25-04-2020 [Consulta: 2 maig 2020].
- ↑ Blanchfield, Mike «Global philanthropists, experts call for COVID-19 vaccine distribution plan». The Toronto Star, 30-04-2020 [Consulta: 6 maig 2020].
- ↑ Stevis-Gridneff, Matina; Jakes, Lara «World Leaders Join to Pledge $8 Billion for Vaccine as U.S. Goes It Alone» (en anglès). The New York Times, 04-05-2020 [Consulta: 10 maig 2020].
- ↑ Jennings, Katie. «How Much Will A Covid-19 Vaccine Cost?» (en anglès). Forbes, 17-11-2020. [Consulta: 6 desembre 2020].
- ↑ Hope, Alan. «European vaccine prices revealed in Belgian Twitter blunder» (en anglès). The Brussels Times, 18-12-2020. [Consulta: 19 desembre 2020].
- ↑ Bossaert, Jeroen. «Zoveel gaan we betalen voor de coronavaccins: staatssecretaris zet confidentiële prijzen per ongeluk online» (en holàndès). Het Laatste Nieuws, 17-12-2020. [Consulta: 18 desembre 2020].
- ↑ 346,0 346,1 Pfizer/BioNTech. «Pfizer-BioNTech COVID-19 Vaccine Vaccination Storage & Dry Ice Safety Handling» (en anglès). Product Storage & Dry Ice, 2021; Ag (rev). Arxivat de l'original el 24 de gener 2021. [Consulta: 28 agost 2021].
- ↑ Branswell, H; Siverman, E. «7 looming questions about the rollout of a Covid-19 vaccine» (en anglès). Health, STAT, 09-10-2020. [Consulta: 10 octubre 2020].
- ↑ FDA Media. «Fact Sheet for Healthcare Providers Administering Vaccine (Vaccination Providers). Emergency Use Authorization (EUA) of the Moderna COVID-19 Vaccine to Prevent Coronavirus Disease 2019 (COVID-19)» (en anglès). ModernaTX, Inc., 24 juny 2021 (rev). [Consulta: 11 juliol 2021].
- ↑ 349,0 349,1 Wee, Sui-Lee. «Chinese Covid-19 Vaccine Gets Key Push, but Doubts Swirl» (en anglès). The New York Times, 09-12-2020. [Consulta: 21 desembre 2020].
- ↑ AFP. «Abu Dhabi starts COVID-19 vaccinations» (en anglès). Arab News, 14-12-2020. [Consulta: 17 desembre 2020].
- ↑ Cyranoski, David «Arab nations first to approve Chinese COVID vaccine — despite lack of public data» (en anglès). Nature, 2020 Des; 588 (7839), pp: 548. DOI: 10.1038/d41586-020-03563-z. ISSN: 1476-4687. PMID: 33318701 [Consulta: 21 desembre 2020].
- ↑ Kertscher, Tom. «No, there is no vaccine for the Wuhan coronavirus» (en anglès). PolitiFact, Poynter Institute for Media Studies, 23-01-2020. [Consulta: 27 febrer 2020].
- ↑ McDonald, Jessica. «Social Media Posts Spread Bogus Coronavirus Conspiracy Theory» (en anglès). Annenberg Public Policy Center of the University of Pennsylvania, 24-01-2020. [Consulta: 8 febrer 2020].
- ↑ Susarla, Anjana. «Big tech has a vaccine misinformation problem – here's what a social media expert recommends» (en anglès). The Conversation, 29-07-2021. [Consulta: 26 octubre 2021].
- ↑ Weinzierl, MA; Harabagiu, SM «Automatic detection of COVID-19 vaccine misinformation with graph link prediction» (en anglès). J Biomed Inform, 2021 Des; 124, pp: 103955. DOI: 10.1016/j.jbi.2021.103955. PMC: 8598278. PMID: 34800722 [Consulta: 3 gener 2022].
Bibliografia
[modifica]- Koff, Wayne C.; Schenkelberg, Theodore; Williams, Tere; Baric, Ralph S.; et al Development and deployment of COVID-19 vaccines for those most vulnerable (en anglès). Sci Transl Med, 2021 Feb 3; 13 (579), pp: eabd1525. PMID: 33536277. DOI 10.1126/scitranslmed.abd1525 [Consulta: 11 juliol 2021].
- Klasse, Per Johan; Nixon, Douglas F.; Moore, John P. Immunogenicity of clinically relevant SARS-CoV-2 vaccines in nonhuman primates and humans (en anglès). Sci Adv, 2021 Mar 19; 7 (12), pp: eabe8065. PMID: 33608249. DOI 10.1126/sciadv.abe8065 [Consulta: 10 juliol 2021].
- Bayat, Maryam; Asemani, Yahya; Najafi, Sajad. Essential considerations during vaccine design against COVID-19 and review of pioneering vaccine candidate platforms (en anglès). Int Immunopharmacol, 2021 Abr 15; 97, pp: 107679. PMID: 33930707. DOI 10.1016/j.intimp.2021.107679 [Consulta: 11 juliol 2021].
- Nagy, Abdou; Alhatlani, Bader. An overview of current COVID-19 vaccine platforms (en anglès). Comput Struct Biotechnol J, 2021 Abr 17; 19, pp: 2508-2517. PMID: 33936564. DOI 10.1016/j.csbj.2021.04.061 [Consulta: 15 agost 2021].
- García-Montero, Cielo; Fraile-Martínez, Oscar; Bravo, Coral; Torres-Carranza, Diego; et al. An Updated Review of SARS-CoV-2 Vaccines and the Importance of Effective Vaccination Programs in Pandemic Times (en anglès). Vaccines (Basel), 2021 Abr 27; 9 (5), pp: 433. PMID: 33925526. DOI 10.3390/vaccines9050433 [Consulta: 11 juliol 2021].
- Arashkia, Arash; Jalilvand, Somayeh; Mohajel, Nasir; Afchangi, Atefeh; et al. Severe acute respiratory syndrome-coronavirus-2 spike (S) protein based vaccine candidates: State of the art and future prospects (en anglès). Rev Med Virol, 2021 Maig; 31 (3), pp: e2183. PMID: 33594794. DOI 10.1002/rmv.2183 [Consulta: 28 setembre 2021].
- Mathieu, Edouard; Ritchie, Hannah; Ortiz-Ospina, Esteban; Roser, Max; et al. A global database of COVID-19 vaccinations (en anglès). Nat Hum Behav, 2021 Maig 10; 5, pp: 947–953. ISSN 2397-3374. DOI 10.1038/s41562-021-01122-8 [Consulta: 6 agost 2021].
- Robinson, Jared; Leclezio, Alexandra; Banerjee, Indrajit. COVID-19: Intranasal and Oral Routes of Vaccination (en anglès). J Lumbini Med Coll, 2021 Maig 10; 9 (1), pp: 1-3. ISSN 2392-4632. DOI 10.22502/jlmc.v9i1.427 [Consulta: 2 octubre 2021].
- Noh, Ji Yun; Jeong, Hye Won; Shin, Eui-Cheol. SARS-CoV-2 mutations, vaccines, and immunity: implication of variants of concern (en anglès). Signal Transduct Target Ther, 2021 Maig 22; 6 (1), pp: 203. PMID: 34023862. DOI 10.1038/s41392-021-00623-2 [Consulta: 18 juliol 2021].
- Lacsa, Jose Eric M.; Cordero, Jr, Dalmacito A. We are here…so where’s the vaccine? Achieving ‘herd immunity’ in the midst of the COVID-19 pandemic (en anglès). J Public Health (Oxf), 2021; Jun 3, pp: fdab195. PMID: 34086967. DOI 10.1093/pubmed/fdab195 [Consulta: 24 juliol 2021].
- Bhat, Amarnath; Browning-McNee, Lea Ann; Ghauri, Kanwal; Winckler, Susan. COVID-19 vaccine confidence project (en anglès). J Am Pharm Assoc (2003), 2021; Jun 11, pp: S1544-3191(21)00273-9. PMID: 34246577. DOI 10.1016/j.japh.2021.06.006 [Consulta: 16 juliol 2021].
- Shimabukuro, Tom T.; Kim, Shin Y.; Myers, Tanya R.; Moro, Pedro L.; et al Preliminary Findings of mRNA Covid-19 Vaccine Safety in Pregnant Persons (en anglès). N Engl J Med, 2021 Jun 17; 384 (24), pp: 2273-2282. PMID: 33882218. DOI 10.1056/NEJMoa2104983 [Consulta: 14 juliol 2021].
- Chen, Musha; Yuan, Yue; Zhou, Yiguo; Deng, Zhaomin; et al. Safety of SARS-CoV-2 vaccines: a systematic review and meta-analysis of randomized controlled trials (en anglès). Infect Dis Poverty, 2021 Jul 5; 10 (1), pp: 94. PMID: 34225791. DOI 10.1186/s40249-021-00878-5 [Consulta: 10 juliol 2021].
- Subbarao, Kanta. The success of SARS-CoV-2 vaccines and challenges ahead (en anglès). Cell Host Microbe, 2021 Jul 14; 29 (7), pp: 1111-1123. PMID: 34265245. DOI 10.1016/j.chom.2021.06.016 [Consulta: 23 juliol 2021].
- Álvarez, Mario Moisés; Bravo-González, Sergio; Trujillo-de Santiago, Grissel. Modeling vaccination strategies in an Excel spreadsheet: Increasing the rate of vaccination is more effective than increasing the vaccination coverage for containing COVID-19 (en anglès). Plos One, 2021 Jul 19; 16 (7), pp: e0254430. PMID: 34280210. DOI 10.1371/journal.pone.0254430 [Consulta: 22 juliol 2021].
- Sen-Crowe, Brendon; McKenney, Mark; Elkbuli, Adel. Disparities in global COVID-19 vaccination rates & allocation of resources to countries in need (en anglès). Ann Med Surg (Lond), 2021; Jul 28, pp: 102620. PMID: 34336193. DOI 10.1016/j.amsu.2021.102620 [Consulta: 4 agost 2021].
- Chavda, Vivek P.; Vora, Lalitkumar K.; Pandya, Anjali K.; Patravale, Vandana B. Intranasal vaccines for SARS-CoV-2: From challenges to potential in COVID-19 management (en anglès). Drug Discov Today, 2021; Jul 29, pp: S1359-6446(21)00331-7. PMID: 34332100. DOI 10.1016/j.drudis.2021.07.021 [Consulta: 28 setembre 2021].
- Pavord, Sue; Scully, Marie; Hunt, Beverley J.; Lester, William; et al. Clinical Features of Vaccine-Induced Immune Thrombocytopenia and Thrombosis (en anglès). N Engl J Med, 2021; Ag 11, pp: 1-10. ISSN 1533-4406. DOI 10.1056/NEJMoa2109908 [Consulta: 12 agost 2021].
- Skelly, Donal T.; Harding, Adam C.; Gilbert-Jaramillo, Javier; Knight, Michael L.; et al Two doses of SARS-CoV-2 vaccination induce robust immune responses to emerging SARS-CoV-2 variants of concern (en anglès). Nat Commun, 2021 Ag 17; 12 (1), pp: 5061. PMID: 34404775. DOI 10.1038/s41467-021-25167-5 [Consulta: 23 agost 2021].
- Iversen, Patrick L.; Bavari, Sina. Extending the interval of COVID-19 vaccine regimens in individuals aged 80 years or older (en anglès). Lancet Healthy Longev, 2021; Ag 19, pp: 1-2. PMID: 34430953. DOI 10.1016/S2666-7568(21)00205-1 [Consulta: 28 agost 2021].
- Niebel, Dennis; Novak, Natalija; Wilhelmi, Jasmin; Ziob, Jana; et al. Cutaneous Adverse Reactions to COVID-19 Vaccines: Insights from an Immuno-Dermatological Perspective (en anglès). Vaccines (Basel), 2021 Ag 25; 9 (9), pp: 944. PMID: 34579181. DOI 10.3390/vaccines9090944 [Consulta: 4 novembre 2021].
- Geng, Qibin; Tai, Wanbo; Baxter, Victoria K.; Shi, Juan; et al. Novel virus-like nanoparticle vaccine effectively protects animal model from SARS-CoV-2 infection (en anglès). PLoS Pathog, 2021 Set 7; 17 (9), pp: e1009897. PMID: 34492082. DOI 10.1371/journal.ppat.1009897 [Consulta: 9 setembre 2021].
- Thura, Min; Sng, Joel Xuan E.; Ang, Koon Hwee; Li, Jie; et al. Targeting Intra-Viral Conserved Nucleocapsid (N) Proteins as Novel Vaccines against SARS-CoVs (en anglès). Biosci Rep, 2021; Set 14, pp: BSR20211491. PMID: 34519332. DOI 10.1042/BSR20211491 [Consulta: 16 setembre 2021].
- Xia, ShengLi; Zhang, YunTao; Wang, YanXia; Wang, Hui; et al. Safety and immunogenicity of an inactivated COVID-19 vaccine, BBIBP-CorV, in people younger than 18 years: a randomised, double-blind, controlled, phase 1/2 trial (en anglès). Lancet Infect Dis, 2021; Set 15, pp: S1473-3099(21)00462-X. PMID: 34536349. DOI 10.1016/S1473-3099(21)00462-X [Consulta: 3 octubre 2021].
- Lara-Puente, Jesús Horacio; Carreño, Juan Manuel; Sun, Weina; Suárez-Martínez, Alejandro; et al. Safety and Immunogenicity of a Newcastle Disease Virus Vector-Based SARS-CoV-2 Vaccine Candidate, AVX/COVID-12-HEXAPRO (Patria), in Pigs (en anglès). mBio, 2021; Set 21, pp: e0190821. PMID: 34544278. DOI 10.1128/mBio.01908-21 [Consulta: 24 setembre 2021].
- Formica, Neil; Mallory, Raburn; Albert, Gary; Robinson, Michelle; et al. Different dose regimens of a SARS-CoV-2 recombinant spike protein vaccine (NVX-CoV2373) in younger and older adults: A phase 2 randomized placebo-controlled trial (en anglès). PLoS Med, 2021 Oct 1; 18 (10), pp: e1003769. PMID: 34597298. DOI 10.1371/journal.pmed.1003769 [Consulta: 12 octubre 2021].
- Gil-Manso, Sergio; Carbonell, Diego; López-Fernández, Luis; Miguens, Iria; et al. Induction of High Levels of Specific Humoral and Cellular Responses to SARS-CoV-2 After the Administration of Covid-19 mRNA Vaccines Requires Several Days (en anglès). Front Immunol, 2021 Oct 4; 12, pp: 726960. PMID: 34671348. DOI 10.3389/fimmu.2021.726960 [Consulta: 23 octubre 2021].
- Carreño, Juan Manuel; Alshammary, Hala; Singh, Gagandeep; Raskin, Ariel; et al. Evidence for retained spike-binding and neutralizing activity against emerging SARS-CoV-2 variants in serum of COVID-19 mRNA vaccine recipients (en anglès). EBioMedicine, 2021 Oct 20; 73, pp: 103626. PMID: 34688034. DOI 10.1016/j.ebiom.2021.103626 [Consulta: 26 octubre 2021].
- Nioi, Matteo; Napoli, Pietro Emanuele. The Waiver of Patent Protections for COVID-19 Vaccines During the Ongoing Pandemic and the Conspiracy Theories: Lights and Shadows of an Issue on the Ground (en anglès). Front Med (Lausanne), 2021 Nov 4; 8, pp: 756623. PMID: 34805221. DOI 10.3389/fmed.2021.756623 [Consulta: 23 novembre 2021].
- Ndeupen, Sonia; Qin, Zhen; Jacobsen, Sonya; Bouteau, Aurélie; et al. The mRNA-LNP platform's lipid nanoparticle component used in preclinical vaccine studies is highly inflammatory (en anglès). iScience, 2021; Nov 20, pp: 103479. PMID: 34841223. DOI 10.1016/j.isci.2021.103479 [Consulta: 1r desembre 2021].
- Ameratunga, Rohan; Woon, See-Tarn; Sheppard, Mary N.; Garland, Jack; et al. First Identified Case of Fatal Fulminant Necrotizing Eosinophilic Myocarditis Following the Initial Dose of the Pfizer-BioNTech mRNA COVID-19 Vaccine (BNT162b2, Comirnaty): an Extremely Rare Idiosyncratic Hypersensitivity Reaction (en anglès). J Clin Immunol, 2022; Gen 3, pp: 1-7. PMID: 34978002. DOI 10.1007/s10875-021-01187-0 [Consulta: 4 gener 2022].
Vegeu també
[modifica]Enllaços externs
[modifica]- «Vacuna COVID-19». Canal Salut. Generalitat de Catalunya.
- SARS-CoV-2 Vaccines and Variants The Rockefeller University. 2021 Feb (en anglès)