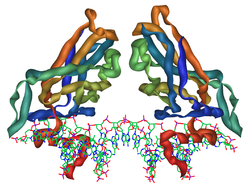
TBR1
 | |
| Substància | gen |
|---|---|
| Subclasse de | gen codificador de proteïnes |
| Massa molecular | 74053 Da |
| Descobridor o inventor | The Nina Ireland Laboratory Of Developmental Neurology |
| Data de descobriment | 1995 |
| Identificadors | |
| Símbol | TBR1 |
| HUGO | 11590 |
| Entrez | 10716 |
| OMIM | 604616 |
| RefSeq | NM_006593.4 |
La proteïna TBR1 (T-Box Brain Transcription Factor 1) és un factor de transcripció que forma part de la família de les proteïnes TBR (T-box brain). També és coneguda amb el nom de TES-56.[6]

La proteïna TBR1 és determinant per a un correcte desenvolupament cerebral i per a la diferenciació de diverses cèl·lules. Una anomalia d'aquesta proteïna pot resultar fatal, ja que pot alterar el funcionament de cèl·lules que es troben a l'escorça cerebral.[7]
Descobriment
[modifica]La proteïna TBR1 va ser descoberta pel Nina Ireland Laboratory of Developmental Neurobiology de San Francisco, un centre d'investigació focalitzat en l'estudi de la neurociència, l'any 1995. El descobriment de la proteïna es va produir en un estudi del centre enfocat a la recerca dels diversos mecanismes biològics encarregats de regular l'evolució de l'escorça cerebral i de controlar la seva especificitat.[8]
Gen TBR1 humà i proteïna codificada
[modifica]Característiques generals
[modifica]És una proteïna que duu a terme funcions molt específiques dins de la cèl·lula. Es calcula que està formada per uns 682 aminoàcids, fet que provoca que tingui una massa molecular de 74053 Da. Es tracta d'una proteïna que trobem en estructura quaternària,[6] formant homodímers.
Característiques genètiques
[modifica]El gen que sintetitza la proteïna TBR1 humana es localitza al braç q de la cadena positiva del cromosoma 2 del genoma humà. Concretament, es troba en la localització: 2q24.2.[9]Presenta les coordenades genòmiques següents: (GRCh38): 2:161,416,297-161,425,871. Té 8.954 parells de bases nitrogenades i presenta 6 exons.[10]

Aquest gen és comú en diverses proteïnes del tipus T-box brain (o TBR) ja que totes elles formen part d'una mateixa família gènica. Això implica que totes les proteïnes d'aquesta família presentin un mateix domini d'unió al DNA.[11] La subfamília de gens T-box està formada per tres gens: TBR1 (conegut com a T-Brain 1 i TES-56), TBR2 i TBX21.[8]
El gen que codifica la TBR1 està present en diversos animals vertebrats, fent que siguin gens ortòlegs. El gen de la proteïna humana TBR1 presenta un 99,9% de similituds amb el mateix gen dels ratolins.[9]
Funcions
[modifica]La proteïna TBR1 és un homòleg del factor de transcripció T-box T (conegut com la proteïna Brachyury), de la família Brachyury, només es coneix que TBR1 s'expressi àmpliament al Sistema Nerviós Central dels vertebrats. TBR1 és un factor de transcripció essencial pel funcionament del cervell: intervé en la regulació de la transcripció de gens en l'ARNm, mitjançant la unió amb l'ADN, i es manifesta en les neurones de projecció postmitòtica del prosencèfal.[12]
Les funcions de TBR1 són vàries: regula el desenvolupament cortical, participa en la guia de l’axó, en la diferenciació neuronal, en la modulació de NMDAR i en la regulació del gen Fezf2.
Guia de l’axó
El factor de transcripció TBR1 està implicat en la migració neuronal en el desenvolupament primerenc de l'escorça cerebral. TBR1 regula l’expressió del gen RELN el qual codifica per a la Reelina, una proteïna de la matriu extracel·lular. TBR1 regula, per tant, la generació de la matriu a través de la qual migren les neurones. L’absència de TBR1 té com a conseqüència que les neurones no migrin correctament.[7]
Diferenciació neuronal
La diferenciació de neurones de projecció glutamatèrgica es realitza gràcies a TBR1, conjuntament amb Pax6 i TBR2 (ambdós factors de transcripció). La producció i alliberació del neurotransmissor excitatori glutamat es deu a les neurones glutamatèrgiques. La transició de les cèl·lules glials radials a les neurones de projecció postmitòtiques succeeix en tres passos associats als factors de transcripció prèviament esmentats, TBR1 és indispensable per la realització del darrer pas, ja que assenyala la transició a una neurona de projecció postmitòtica.[13]
Modulació de NMDAR
TBR1 interacciona amb CINAP (proteïna d'acoblament del nucleosoma), en les neurones hipocampals cultivades, per tal d’executar l'expressió de la subunitat 2b del receptor de l'àcid N-metil-D -aspàrtic (NR2b), actuant sobre la seva regió promotora.[14] A més, TBR1 intervé en la regulació transcripcional d'una subunitat dels receptors NMDA.[15]
Regulació del gen Fezf2
Una de les funcions de TBR1 és actuar com a repressor transcripcional del gen Fezf2, el que comporta que el tracte corticoespinal pugui tenir el seu origen laminar a la capa 5 (l'escorça cerebral està constituïda per sis capes).
El tracte corticoespinal és la via primària per les ordres motores implicades en el control de moviments discrets voluntaris dels mamífers i el seu desenvolupament està lligat al gen Fezf2. El factor de transcripció TBR1, que s’expressa a la capa 6, és capaç d’unir-se específicament al locus d’aquest gen i reprimir la seva expressió, de manera que l’origen del tracte queda restringit a les neurones de projecció de la capa 5 (on sí que es pot expressar lliurement el gen).[16][17]
Inhibició
[modifica]La inhibició de TBR1 depèn de les concentracions de CTIP1, proteïna coexpressada amb CTIP 2 (en neurones que es projecten a objectius subcerebrals), formant un dímer, i amb SATB2 (en neurones que es projecten a l’escorça contra lateral). D’aquesta manera CTIP1 és capaç d’inhibir l’acció de TBR1. És per això que cal una major concentració de CTIP a la capa 5 i, contràriament, una menor concentració a la 6, ja que de no ser així, hi hauria una malformació del tracte corticoespinal.

Un altre mecanisme per a la inhibició de TBR1 és la que està regulada per la proteïna AF-9, la qual està implicada en la formació de l’escorça cerebral mitjançant la supressió de TBR1 a les capes superiors. La supressió està basada en la interacció que s’estableix entre AF-9 i DOT1L (proteïna que regula el control transcripcional). AF-9 és capaç d’interferir amb l’activitat de l’ARN polimerasa en el lloc d’inici transcripcional de TBR1, gràcies al fet que s’associa a aquest lloc mitjançant la dimetilació (l'addició de dos grups metils) de la histona H3 lisina 79 (H3K79) del gen TBR1 produint, d’aquesta manera, una reducció en l’expressió de TBR1.[18]
Complex CASK- CINAP - TBR1
[modifica]La proteïna CASK (serina proteïna quinasa dependent del calci) pot actuar com un coactivador del factor de transcripció TBR1 per a regular l’expressió d’alguns gens. Per fer-ho, CASK s’uneix a la proteïna nuclear CINAP, la qual s’uneix a histones i facilita l’assemblatge de nucleosomes.[19]
Gràcies a les interaccions amb la proteïna CASK, CINAP és capaç de formar un complex amb TBR1 permetent la regulació de gens diana de TBR1, com NR2b o RELN. Aquest últim sintetitzarà la proteïna Reelina, decisiva en la regulació de processos de migració neuronal durant el desenvolupament del cervell en estat embrionari[20]
Localització cel·lular
[modifica]Es tracta d’un factor de transcripció i, per tant, actua en regions concretes del DNA per facilitar la transcripció de gens concrets. Per aquest motiu, dins la cèl·lula, trobarem la proteïna TBR1 al nucli,[11] on duu a terme la seva funció principal.
Localització al cos (Teixits)
[modifica][7]Trobem aquesta proteïna majoritàriament al nucli de les cèl·lules glutamatèrgiques del còrtex cerebral però no en les cèl·lules gabaèrgiques. La TBR1 es pot observar en cèl·lules glutamatèrgiques postmitòtiques de la subplaca i la capa 6 de l'escorça cerebral. No obstant això, tenim constància de què aquesta proteïna també és present en altres zones com l'hipotàlem, la zona ventricular i les amígdales cerebrals. Fins i tot, es poden trobar a les cèl·lules del bulb olfactori.[21][22]
Malalties lligades amb el gen i/o la proteïna Tbr1
[modifica]Una mala expressió del gen que codifica la proteïna TBR1 (o per defecte, la seva mutació, deleció o traducció errònia); pot donar lloc a proteïnes TBR1 defectuoses que presentaran una seqüència d'aminoàcids incorrecta (que no es correspon amb el que hi ha codificat al DNA) o que estan mal plegades.[23][24]
Aquestes proteïnes defectuoses són la causa de diversos trastorns relacionats amb el desenvolupament neuronal i cerebral.
Una d'aquestes malalties és el trastorn lligat al gen TBR1, una malaltia minoritària que no arriba a la cinquantena d'afectats. Es tracta d'una malaltia sense cura que presenta greus trastorns lligats al desenvolupament cerebral. Els afectats poden presentar una discapacitat intel·lectual, trastorns en el comportament, dificultats en l'expressió verbal, etc.[23]Altrament, també s'han trobat persones afectades pel trastorn de l'espectre autista que mostren mutacions en el gen que codifica la proteïna TBR1.[25][24]En aquests casos, si es produeix una mutació patògena es pot patir també una discapacitat intel·lectual, un impediment del llenguatge o fins i tot petits canvis estructurals en determinades zones com l'hipocamp.[26][27] També, s'ha observat com una proteïna TBR1 defectuosa pot estar relacionada i ser una de les causants de malalties com el Parkinson i l'Alzheimer.[11]
Finalment, s'ha observat com l'exposició i el consum de cocaïna en estadis embrionaris primerencs poden causar danys al fetus provocant un retard en l'expressió de TBR1, entre altres efectes.[28]
Tanmateix, encara falta molta informació sobre els efectes de la proteïna TBR1 quan és defectuosa, ja que en la gran majoria de diagnòstics no es fa un estudi genètic que ens permeti establir una relació.[29][27]
Referències
[modifica]- ↑ «Malalties que s'associen genèticament amb TBR1, vegeu/editeu les referències a wikidata».
- ↑ 2,0 2,1 2,2 GRCh38: Ensembl release 89: ENSG00000136535 - Ensembl, May 2017
- ↑ 3,0 3,1 3,2 GRCm38: Ensembl release 89: ENSMUSG00000035033 – Ensembl, May 2017
- ↑ «Human PubMed Reference:». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ «Mouse PubMed Reference:». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ 6,0 6,1 Fishilevich, Simon; Zimmerman, Shahar; Kohn, Asher; Iny Stein, Tsippi; Olender, Tsviya «Genic insights from integrated human proteomics in GeneCards» (en anglès). Database, 2016, 2016, pàg. baw030. DOI: 10.1093/database/baw030. ISSN: 1758-0463.
- ↑ 7,0 7,1 7,2 Hevner, Robert F; Shi, Limin; Justice, Nick; Hsueh, Yi-Ping; Sheng, Morgan «Tbr1 Regulates Differentiation of the Preplate and Layer 6». Neuron, 29, 2, 2-2001, pàg. 353–366. DOI: 10.1016/s0896-6273(01)00211-2. ISSN: 0896-6273.
- ↑ 8,0 8,1 Bulfone, Alessandro; Smiga, Susan M.; Shimamura, Kenji; Peterson, Andrew; Puelles, Luis «T-Brain-1: A homolog of Brachyury whose expression defines molecularly distinct domains within the cerebral cortex» (en anglès). Neuron, 15, 1, 7-1995, pàg. 63–78. DOI: 10.1016/0896-6273(95)90065-9.
- ↑ 9,0 9,1 «T-BOX, BRAIN, 1; TBR1» (en en anglès). OMMIM, 25-02-2000.
- ↑ «TBR1 T-box brain transcription factor 1 [Homo sapiens (human) - Gene - NCBI]».
- ↑ 11,0 11,1 11,2 Andrews, Lin «On the Spectrum with T‐box Brain Protein 1: A Transcription Factor Protein Critical for Normal Neural Development» (en anglès). The FASEB Journal, 33, S1, 4-2019. DOI: 10.1096/fasebj.2019.33.1_supplement.lb200. ISSN: 0892-6638.
- ↑ Scholz, Corinna B.; Technau, Ulrich «The ancestral role of Brachyury: expression of NemBra1 in the basal cnidarian Nematostella vectensis (Anthozoa)» (en anglès). Development Genes and Evolution, 212, 12, 1-2003, pàg. 563–570. DOI: 10.1007/s00427-002-0272-x. ISSN: 0949-944X.
- ↑ Englund C, Fink A, Lau C, Pham D, Daza RA, Bulfone A, Kowalczyk T, Hevner RF. «Pax6, Tbr2, and Tbr1 are expressed sequentially by radial glia, intermediate progenitor cells, and postmitotic neurons in developing neocortex». The Journal of Neuroscience, 25, 1, (Jan 2005), pàg. 247–51. DOI: 10.1523/JNEUROSCI.2899-04.2005.. PMC: 6725189.. PMID: 15634788..
- ↑ Chung, Wen-Chuan; Huang, Tzyy-Nan; Hsueh, Yi-Ping «Targeted Deletion of CASK-Interacting Nucleosome Assembly Protein Causes Higher Locomotor and Exploratory Activities» (en anglès). Neurosignals, 19, 3, 2011, pàg. 128–141. DOI: 10.1159/000327819. ISSN: 1424-8638.
- ↑ Wang, Ting-Fang; Ding, Chia-Nung; Wang, Guey-Shin; Luo, Shih-Chi; Lin, Yi-Ling «Identification of Tbr-1/CASK complex target genes in neurons: Target genes of Tbr-1/CASK complex» (en anglès). Journal of Neurochemistry, 91, 6, 02-12-2004, pàg. 1483–1492. DOI: 10.1111/j.1471-4159.2004.02845.x.
- ↑ Han, Wenqi; Kwan, Kenneth Y.; Shim, Sungbo; Lam, Mandy M. S.; Shin, Yurae «TBR1 directly represses Fezf2 to control the laminar origin and development of the corticospinal tract» (en anglès). Proceedings of the National Academy of Sciences, 108, 7, 15-02-2011, pàg. 3041–3046. DOI: 10.1073/pnas.1016723108. ISSN: 0027-8424.
- ↑ McKenna, W. L.; Betancourt, J.; Larkin, K. A.; Abrams, B.; Guo, C. «Tbr1 and Fezf2 Regulate Alternate Corticofugal Neuronal Identities during Neocortical Development» (en anglès). Journal of Neuroscience, 31, 2, 12-01-2011, pàg. 549–564. DOI: 10.1523/JNEUROSCI.4131-10.2011. ISSN: 0270-6474.
- ↑ Büttner, Nicole; Johnsen, Steven A.; Kügler, Sebastian; Vogel, Tanja «Af9/Mllt3 interferes with Tbr1 expression through epigenetic modification of histone H3K79 during development of the cerebral cortex» (en anglès). Proceedings of the National Academy of Sciences, 107, 15, 13-04-2010, pàg. 7042–7047. DOI: 10.1073/pnas.0912041107. ISSN: 0027-8424.
- ↑ Wang GS, Hong CJ, Yen TY, Huang HY, Ou Y, Huang TN, Jung WG, Kuo TY, Sheng M, Wang TF, Hsueh YP «"Transcriptional modification by a CASK-interacting nucleosome assembly protein".». Neuron. 42 (1):, (Apr 2004)., pàg. 113–28.. DOI: 10.1016/S0896-6273(04)00139-4.. PMID: 15066269..
- ↑ Hsueh, Yi-Ping; Wang, Ting-Fang; Yang, Fu-Chia; Sheng, Morgan «Nuclear translocation and transcription regulation by the membrane-associated guanylate kinase CASK/LIN-2» (en anglès). Nature, 404, 6775, 16-03-2000, pàg. 298–302. DOI: 10.1038/35005118. ISSN: 0028-0836.
- ↑ «TBR1 (T-box brain transcription factor 1)». [Consulta: 28 octubre 2022].
- ↑ Sjöstedt, Evelina; Zhong, Wen; Fagerberg, Linn; Karlsson, Max; Mitsios, Nicholas «An atlas of the protein-coding genes in the human, pig, and mouse brain» (en anglès). Science, 367, 6482, 06-03-2020, pàg. eaay5947. DOI: 10.1126/science.aay5947. ISSN: 0036-8075.
- ↑ 23,0 23,1 «TBR1-related disorder"». Unique: Understanding Chromosome & Gene Disorders.Version 1 [AP], Version 1.1 [AP]., 2020.
- ↑ 24,0 24,1 Huang, Tzyy-Nan; Chuang, Hsiu-Chun; Chou, Wen-Hsi; Chen, Chiung-Ya; Wang, Hsiao-Fang «Tbr1 haploinsufficiency impairs amygdalar axonal projections and results in cognitive abnormality» (en anglès). Nature Neuroscience, 17, 2, 2-2014, pàg. 240–247. DOI: 10.1038/nn.3626. ISSN: 1097-6256.
- ↑ McDermott, J.H.; Study, D.D.D.; Clayton-Smith, J.; Briggs, T.A. «The TBR1 -related autistic-spectrum-disorder phenotype and its clinical spectrum» (en anglès). European Journal of Medical Genetics, 61, 5, 5-2018, pàg. 253–256. DOI: 10.1016/j.ejmg.2017.12.009.
- ↑ den Hoed, Joery; Sollis, Elliot; Venselaar, Hanka; Estruch, Sara B.; Deriziotis, Pelagia «Functional characterization of TBR1 variants in neurodevelopmental disorder» (en anglès). Scientific Reports, 8, 1, 12-2018, pàg. 14279. DOI: 10.1038/s41598-018-32053-6. ISSN: 2045-2322.
- ↑ 27,0 27,1 CAUSES Study; Nambot, Sophie; Faivre, Laurence; Mirzaa, Ghayda; Thevenon, Julien «De novo TBR1 variants cause a neurocognitive phenotype with ID and autistic traits: report of 25 new individuals and review of the literature» (en anglès). European Journal of Human Genetics, 28, 6, 6-2020, pàg. 770–782. DOI: 10.1038/s41431-020-0571-6. ISSN: 1018-4813.
- ↑ V. Gonzalez-Nunez, R.E. Rodríguez. The Neuroscience of Cocaine. Capítol 12. Academic Press, 2017, p. 107-124. DOI 10.1016/B978-0-12-803750-8.00012-9. ISBN 9780128037508.
- ↑ Sapey-Triomphe, Laurie-Anne; Reversat, Julie; Lesca, Gaëtan; Chatron, Nicolas; Bussa, Marina «A de novo frameshift pathogenic variant in TBR1 identified in autism without intellectual disability» (en anglès). Human Genomics, 14, 1, 12-2020, pàg. 32. DOI: 10.1186/s40246-020-00281-5. ISSN: 1479-7364.